커피의 쓴맛물질 4-비닐카테콜 올리고머 (Bitter-Tasting 4-Vinylcatechol Oligomers in Roasted Coffee)

KEYWORDS: Coffee; bitter taste; taste dilution analysis; caffeic acid; chlorogenic acid; 5-O-caffeoylquinic acid;
phenylindanes; 4-vinylcatechol; polyphenols
Abstract
- 커피의 강렬한 쓴맛 내는 분자들의 규명에 목적을 두고,
여러 콩 성분들이 모델 실험들에서 열처리되었고, 쓴 화합물들을 생산하는 잠재력이 평가되었다. - Caffeic acid (커피酸)가
⇒ 강하게 로스트된 에스프레소 타입 커피의 쓴 맛을 연상시키는
강렬한 쓴맛(intense bitterness)을 생성하는 것으로 발견되었기 때문에,
⇒ 형성되는 그 반응 산물들이 taste dilution analysis에 의하여
bitter compounds에 대해 스크린되었고,
가장 쓴맛 물질들(bitter tastants)이 분리되어 정제되었다. - 1-D/2-D NMR experiments 뿐만 아니라
LC-MS/MS가
⇒ 23~178 µmol/L 사이의 다소 낮은 인식 식역 농도들을 가진
⇒ 10가지 쓴 화합물들의 식별을 가능케 하였다. - 이 bitter compounds는
⇒ 이전에 보고되지 않았던
⇒ ■ 1,3-bis(3′,4′-dihydroxyphenyl) butane,
■ trans-1,3-bis(3′,4′-dihydroxyphenyl)-1-butene, 그리고
■ eight multiply hydroxylated phenylindanes이었고,
⇒ 이들 중 5가지 파생물들이 최초로 보고되었다. - 추가적으로 한 coffee brew 내의 이 bitter compounds 각각의 발생이
⇒ multiple reaction monitoring (MRM) mode에서 작동하는 LC-MS/MS (ESI-)에 의해 검증되었다. - 이 쓴 화합물들의 구조들은,
⇒ 그들이 로스팅 동안에
caffeic acid moieties로부터 발산된
4-vinylcatechol의 oligomerization에 의해서 생성된다는 강한 증거를 보였다.
INTRODUCTION
- 갓 내린 커피 음료의 인기는 그것의 자극 효과 이외에,
주로 매혹적인 아로마의 순수한 향유와 잘 균형 잡힌 테이스트 프로파일 덕분이다. - 지난 15년 내에,
gas chromatography/olfactometry에 의한 냄새물질들에 대한 관능-기반의 스크리닝과,
stable isotope dilution analysis와
aroma reconstitution and omission experiments에 의한 정확한 계량화를
포함하는 현대적인 아로마 연구 전략들이
수백 개의 커피 휘발성 물질들 가운데 30개를 넘지 않는 냄새물질들이
신선하게 추출된 커피의 전형적인 냄새를 모방하는데 필수적으로 필요하다는 것을 인상적으로 밝혀왔다 [1-3]. - 커피 콩의 적절한 로스팅 동안에 발달된
아로마 활성적 휘발성 물질들에 비해, 전형적인 커피 쓴맛의 분자 기준에 관한 지식은 다소 파열적이다. - 20년 이상 전에, 최초의 체계적인 분석 및 관능적 스터디들이
이미 본래의 커피 콩에 존재하는 알카로이드 카페인과 트리고넬린이 각각
커피 음료의 전체 쓴맛 강도의 최대 10-20%, 1%를 차지한다는 것을 밝혔다 [4].
그 저자는 콩 로스팅 동안에 전구물질들로부터 열적으로 생성된 분자들이
커피 추출액 쓴맛의 핵심 유출자(elicitors)라는 것을 제시하고 있다. - 특히
furfurylalcohol [5],
5-hydroxymethyl-2-furanaldehyde [6],
여러 pyrazines [6], 뿐만 아니라,
cis- and trans-configured 2,5-diketopiperazines [7]가
배전커피들 속의 잠재적인 쓴맛나는 물질(potential bitter-tasting agents)로 제시되었지만,
이 헤테로고리 화합물들(heterocyclic compounds)의 경우에
지금까지 커피 쓴맛에 대한 공헌이 확인될 수 있는 것은 없었다. - 그런 헤테로고리 화합물들(heterocyclics) 이외에,
chlorogenic acids으로도 알려진 O-caffeoylquinic acids [8]과 그리고
그들의 상응하는 열적으로 생성된 lactones [9]가
관찰된 커피 쓴맛의 원인으로 논의되었지만,
이 연구들에서는 정제된 화합물을 가지고 관능적으로 평가된 것도 없었고,
사람의 쓴맛 검출 식역들이 결정된 바도 없었다. - 게다가, chlorogenic acid의 열가수분해(thermohydrolysis) 중에
CGA로부터 방출된 quinic acid가
10 ppm의 식역 농도에서 아스피린 같은 쓴맛을 나타내는 것으로 보고된 바 있다. - 배전커피 내에서의 이 화합물의 농도는 그 식역 농도를 20배 만큼 초과하기 때문에,
커피 쓴맛에 대한 공헌물질들 가운데 하나로서 quinic acid가 제시되었다 [10, 11].

- 매우 최근에,
미디엄 로스트된 커피 추출액에 대한 센서리-유도적 분석과
그에 따른 LC-MS/MS와
2-D NMR spectroscopy 및 synthesis가
배전커피 내에서 강하게 쓴맛을 내는 화합물로서 다음의 물질들에 대한 명백한 식별을 이끌어내었다 [12].
■ 3-O-caffeoyl-γ-quinide,
■ 4-O-caffeoyl-γ-quinide,
■ 5-O-caffeoyl-epi-δ-quinide,
■ 4-O-caffeoyl-muco-γ-quinide,
■ 5-O-caffeoyl-muco-γ-quinide,
■ 3-O-feruloyl-γ-quinide, and
■ 4-O-feruloyl-γ- quinide - 이 개별 쓴 화합물들 이외에, 우리는 고도로 복잡하고 쓴 RP-18 fraction을 분리해내고
그 플랙션 내에서의 강하게 쓴맛을 내는 화합물들로서 다음과 같은 물질들을 식별하였다 [12].
■ 3,4-O-dicaffeoyl-γ-quinide,
■ 3,5-O-dicaffeoyl-epi-δ-quinide, and
■ 4,5-O-dicaffeoyl-muco-γ-quinide - 센서리 실험들은, 이 lactones들의 bitter threshold levels가
그 화학구조에 따라 9.8~180 µmol/L (water) 사이의 범위에 달함을 밝혔다 [12]. - The total complex RP-18 fraction의
human bitter threshold concentration (사람의 쓴맛 식역농도)와
dicaffeoylquinides의 식역농도들을 비교한 결과,
이미 식별된 그 화합물들 이외에, 추가적인 물질들이 커피 쓴맛에서 중요한 역할을 한다는 것이 나타났다. - 그 RP-18 fraction의 엄청난 복잡성으로 인하여
추가적인 쓴 화합물들의 성공적인 분리가 어렵기 때문에, - 본 연구의 目的은
⇒ 주요 콩 성분들의 쓴맛 전구물질 잠재력(bitter taste precursor potential)을 평가하고
⇒ 최근에 개발된 taste dilution analysis [13]을 적용하여 가장 쓴 화합물들을 검사하며,
⇒ 인간의 쓴맛 반응을 최고로 유도하는 화합물들을 식별하고, 그리고 마지막으로
⇒ 갓 마련된 커피 추출액 내에서의 이 쓴 화합물들의 발생을
LCMS/MS experiments에 의해 확인하고자 하는 것이었다.
MATERIALS AND METHODS
Chemicals.
- 다음과 같은 화학물질들은 상업적으로 구입되었다 :
caffeic acid, 5-O-caffeoylquinic acid, L-glutamic acid, L-proline, L-alanine,
L-asparagine, L-aspartic acid, quinic acid, sucrose, and trigonelline (Aldrich, Steinheim, Germany) - 그리고 용매들(solvents)은 HPLC grade의 것이었다 (Merck, Darmstadt, Germany).
- DMSO-d6, CDCl3, 그리고 methanol-d4는 Euriso-top (Saarbrücken, Germany)에서 구입되었다.
- 콜롬비아산 아라비카 배전 커피는 커피 업계로부터 구입되었다.
Sensory Analyses.
- 12명의 평가자들(5명의 남성과 7명의 여성)이
본 연구의 센서리 테스트에 참가 동의를 해주었고 알려진 미각장애의 이력을 가진 사람은 없었으며,
적어도 2년 동안 앞서 기술된 바와 같이 정기적인 간격 동안에 센서리 실험들에서 훈련을 받았고
따라서 적용되는 테크닉들에 친숙한 사람들이었다. - 센서리 분석에 앞서, 플랙션들 또는 화합물들을 물에 띄웠고,
고진공(<5 mPa)에서 휘발물질들을 제거한 후에 두번 냉동건조 되었다. - GC-MS and ion chromatographic analysis은
이 절차들에 의해 처리된 푸드 플랙션들이 본질적으로 솔벤트들과 사용된 완충물질들(buffer compounds)이
없음을 나타냈다. - triangle test [18]를 사용하여,
맛 인식 식역농도들(taste recognition threshold concentrations)이
물(Evian, low mineralization: 405 mg/L; pH 5.2) 속에서 결정되었다.
12명의 개인들과 3회의 별도의 세션들 간의 값들은 one dilution step 이상 다르지 않았다.
(즉, 카페인의 경우 0.5 mmol/L의 역치(threshold value)는 0.25에서 1.0 mmol/L 까지의 범위를 나타낸다).
Model Roasting Experiments.
- 5-O-Caffeoylquinic acid,
quinic acid,
caffeic acid,
ferulic acid,
trigonelline, and
sucrose (2.5 mmol each) 그리고
a mixture containing sucrose (2.5 mmol),
L-glutamic acid (0.09 mmol),
L-proline (0.04 mmol),
L-alanine (0.05 mmol),
L-asparagine (0.03 mmol), and
L-aspartate (0.02 mmol)이
별도로 물(3 mL)에 띄워졌고 30 min 동안 80 °C에서 건조되었으며
그 다음에 실험실 오븐에서 15 min 동안 220 °C에서 로스트되었다. - 그 로스팅 결과물들을 hot water (50 mL, 80 °C, pH 5.2)에 녹였다가 상온까지 식혔고
그 다음에 2개의 앨리퀏들(aliquots)로 분할하였다. - 한 앨리퀏(20 mL)은 센서리 분석에 사용되었고
다른 한 앨리퀏(30 mL)은 아세트 에틸(ethyl acetate, 5×50 mL)로 추출되었다(extracted). - 그 결합된 유기물 레이어들(combined organic layers)은
고진공(<5 mPa)에서 솔벤트가 제거되었고
나머지는 methanol/water (1:2, v/v; 20 mL) 혼합물 속에 넣어져
taste dilution analysis, HPLC-DAD, 그리고 HPLC-MS/MS에 의해 분석되었다.
Taste Dilution Analysis (TDA).
- 열처리된 caffeic acid에서 얻어진 solvent extract의 앨리퀏(100 µL)은
250mm × 10mm i.d., 5µm, Microsorb 100-5 C18 column (Varian, Darmstadt, Germany)을 사용하여
a semipreparative RP-18 HPLC에 의해 분리되었다. - 282 nm에서 그 용출물(탈리물)을 모니터링하면서, chromatography가 수행되었는데,
aqueous formic acid (0.1% in water)과 acetonitrile의 혼합물(75:25, v/v)로 시작하여,
5 min 내에 아세토니트릴(acetonitrile)의 함유율을 28%까지 증가시켰고, 그 다음 20 min 내에 30%까지,
그리고 그 다음 5 min 이내에 100%까지 증가시켰고, 마지막으로 추가적인 5 min 동안에는 함유율을 유지시켰다. - Figure 1에 나타난 바와 같이, 10회의 runs에서 얻어진 24개의 상응 fractions가 결합되었다.
- 진공에서 솔벤트를 제거한 후에,
C-18 E cartridges (1g) (Phenomenex, Aschaffenburg, Germany)를 사용하여
RP-18 solid phase extraction에 의하여 개별 플랙션들을 정제하였는데,
이 카트리지들은 사용되기 전에 methanol로 컨디션 되고 그 다음 물로 컨디션되었다. - 샘플 적용 후에, 그 카트리지들을 물(20mL)로 헹궜고 진공 펌프로 15 min 동안 그 카트리지를 통해 질소가 흡입되었으며, 그리고 마지막으로 타겟 화합물을 메탄올 (20mL)로 용리하였다.
- 고진공(<5 mPa)에서 솔벤트를 제거한 후에, 개별 플랙션들을 염산수용액(aqueous hydrochloric acid)(0.1 mol/L)을 사용하여 pH 5.2로 조정된 병입된 물 정확히 2.0mL에 천연 비율들로 용해하였고, 그런 다음에 the taste dilution analysis을 위해 사용하였다 [13-17].
- 이를 달성하기 위해, 개별 용액들을 병입된 물로 순차적으로 1:1 희석하였고, 그 플랙션들 각각의 연속적인 희석물들을 농도가 높아지는 순서대로 센서리 패널들에게 제시하였고 각 희석한 것들을 triangle test에 의해 bitter taste을 평가해달라고 하였다.
- 희석된 추출물(diluted extract)과 blank (control) 간의 맛 차이가 검출될 수 있었던
희석물(dilution)만이 taste dilution으로 정의되었다 [13-17]. - 3회의 다른 세션들에서 4명의 다른 평가자들에 의해 평가된 TD-factors을 평균하였다.
- 개인들과 별도 세션들 간의 TD-factors는 one dilution step 이상 다르지 않았다.

Isolation of Bitter Compounds 1-9a,b from HPLC Fractions 10-15, 17, 20, and 21.
- 열처리된 caffeic acid로부터 얻어진 솔벤트 추출물들을
250mm × 10mm i.d., 5 µm, Microsorb 100-5 C18 column (Varian, Darmstadt, Germany)을 사용하여
semipreparative RP18 HPLC에 의하여 분리하였다. - 282 nm에서 그 용출물들을 모니터링 하면서, chromatography가 수행되었는데,
aqueous formic acid (0.1% in water)과 acetonitrile의 혼합물(75:25, v/v)로 시작하여,
5 min 내에 아세토니트릴(cetonitrile)의 함유율을 28%까지 증가시켰고, 그 다음 20 min 내에 30%까지,
그리고 그 다음 5 min 이내에 100%까지 증가시켰고, 마지막으로 추가적인 5 min 동안에는 함유율을 유지시켰다. - HPLC fractions 10- 15, 17, 20, 21 (Figure 1)이
몇 회의 runs에서 개별적으로 수집되었고, 상응하는 플랙션들의 탈리액들이 결합되었다. - 페놀 맛 화합물들의 산화적 분해를 피하기 위해, 수집된 각 플랙션에 ascorbic acid (0.25 mg/mL)이 더해졌다.
- 진공에서 솔벤트를 제거한 후에, 각 플랙션들을 최종적으로
C-18 E cartridges (1g) (Phenomenex, Aschaffenburg, Germany)를 사용하여
solid phase extraction에 의하여 정제하였다. - 카트리지는 methanol로 컨디션된 다음 water로 컨디션되었다 (20 mL each).
- 샘플 적용 후에, 그 카트리지들을 물(20mL)로 헹궜고
진공 펌프로 15 min 동안 그 카트리지를 통해 질소가 흡입되었으며, 그리고
마지막으로 타겟 화합물을 메탄올 (20mL)로 용리하였다. - 각 개별 플랙션들의 탈리액을 2개의 앨리퀏으로 나누었고, 고진공(<5 mPa)에서 솔벤트를 제거한 후에,
1개의 앨리퀏은 taste threshold concentrations의 결정을 위해 사용되었고,
두 번째 앨리퀏은 구조 결정을 위해 사용되었다. - UV/vis, LC-MS/MS, 그리고 1-D/ 2-D NMR experiments에 의해서,
다음과 같은 테이스트 화합물들(Figure 2)이
98% 이상의 순도에서 brackets에 주어진 HPLC fraction으로부터 분리 되었다 :
compound 1 (11), 2 (12), 3 (13), 4 (14), 5 (15), 6 (17), 7 (20), 8 (21), 9a (10), and 9b (11).

trans-5,6-Dihydroxy-1-methyl-3-(3′,4′-dihydroxyphenyl) indane, 1
(the arbitrary numbering of the carbon atoms refers to the structure given in Figure 2):
UV/vis (water/acetonitrile; 65:35, v/v): λmax 286 nm; LC/TOF-MS: C16H16O4; LC/MS (ESI-): m/z 271.0 (100; [M - H]-); 1H NMR (400 MHz; d3-MeOD; COSY): δ 1.21 [d, 3H, J = 6.80 Hz, H-C(8)], 2.08 [ddd, 1H, J = 5.2, 8.0, 12.8 Hz, H-C(2α)], 2.17 [ddd, 1H, J = 6.0, 7.6, 12.8 Hz, H-C(2β)], 3.14-3.25 [m, 1H, J = 6.7 Hz, H-C(1)], 4.15 [dd, 1H, J = 6.0, 8.0 Hz, H-C(3)], 6.40 [s, 1H, H-C(4)], 6.46 [dd, 1H, J = 2.0, 8.0 Hz, H-C(6′)], 6.50 [d, 1H, J = 2.0 Hz, H-C(2′)], 6.66 [s, 1H, H-C(7)], 6.67 [d, 1H, J = 8.0 Hz, H-C(5′)] ; 13C NMR (100 MHz; d3-MeOD; HMQC, HMBC): δ 19.9 (CH3, C(8)), 37.4 (CH, C(1)), 45.4 (CH2, C(2)), 48.6 (CH, C(3)), 109.6 (CH, C(7)), 111.2 (CH, C(4)), 114.2 (CH, C(2′)), 114.6 (CH, C(5′)), 118.7 (CH, C(6′)), 137.3 (C, C(3a)), 138.2 (C, C(1′)), 140.1 (C, C(1a)), 142.9 (C, C(4′)), 143.7 (C, C(5)), 144.0 (C, C(6)), 144.7 (C, C(3′)).
cis-5,6-Dihydroxy-1-methyl-3-(3′,4′-dihydroxyphenyl) indane, 2 (Figure 2):
UV/vis (water/acetonitrile; 65:35; v/v): λmax 286 nm; LC/ TOF-MS: C16H16O4; LC/MS (ESI-): m/z 271.0 (100; [M -H]-); 1H NMR (400 MHz; d3-MeOD; COSY): δ 1.30 [d, 3H, J = 6.8 Hz, H-C(8)], 1.39-1.51 [m, 1H, J = 10.4, 12.0 Hz, H-C(2α)], 2.60 [ddd, 1H, J = 6.8, 7.2, 12.0 Hz, H-C(2β)], 2.97-3.08 [m, 1H, J = 6.8, 10.0 Hz, H-C(1)], 3.93 [dd, 1H, J = 7.2, 10.4 Hz, H-C(3)], 6.29 [s, 1H, H-C(4)], 6.53 [dd, 1H, J = 2.1, 8.1 Hz, H-C(6′)], 6.61 [d, 1H, J = 2.1 Hz, H-C(2′)], 6.65 [s, 1H, H-C(7)], 6.71 [d, 1H, J = 8.1 Hz, H-C(5′)] ; 13C NMR (100 MHz; d3-MeOD; HMQC, HMBC): δ 19.0 (CH3, C(8)), 37.7 (CH, C(1)), 47.3 (CH2, C(2)), 49.6 (CH, C(3)), 109.2 (CH, C(7)), 111.1 (CH, C(4)), 114.8 (CH, C(2′)), 114.8 (CH, C(5′)), 119.3 (CH, C(6′)), 138.9 (C, C(3a)), 139.6 (C, C(1′)), 141.2 (C, C(1a)), 143.2 (C, C(5)), 144.5 (C, C(4′)), 145.2 (C, C(6)), 146.2 (C, C(3′)).



Preparation of the Coffee Beverage.
- sieve (2 mm pore diameter)를 장착한 울트라 원심분리 밀에 의해 커피 콩을 분쇄한 후,
커피 파우더 앨리쿼트(54 g)를 커피 필터 (No. 4, Melitta, Minden, Germany)에 담았고,
Melitta Look coffee maker (Melitta, Minden, Germany)을 사용하여
여과된 액체(filtrate)가 부피 1L에 달할 때까지 온수로 삼출(percolate)하였다. - 결과적으로 만들어진 음료(54 g/L)는 온도가 75 ℃였고
HPLC-MS/MS analysis 이전에 아이스 배쓰에서 급속하게 냉각되었다.
High-Performance Liquid Chromatography (HPLC).
- HPLC 기기(Kontron, Eching, Germany)는
2개의 422-type pumps, an M800-type gradient mixer, a 100 µL Rheodyne injector, 그리고
a 520-type diode array detector로 구성되었고,
220 and 500 nm 사이의 범위에서 용출물을 모니터하였다. - 분리는
5.2 Ml/min의 유속(flow rate)으로 작동하는
a semipreparative 250mm×10mm
i.d., 5µm, Microsorb 100-5 C18 column (Varian, Darmstadt, Germany) 또는,
1.0 mL/min의 유속으로 작동하는
an analytical 250mm×4.6mm i.d., 5µm, Microsorb 100-5 C18 column에서 수행되었다.
LC/Time-of-Flight Mass Spectrometry (LC/TOF-MS).
- 분리해낸 화합물들 1-9의 High resolution mass spectra가
a Bruker Micro-TOF mass spectrometer (Bruker Daltronics, Bremen, Germany) 상에서 측정되었고
포름산 나트륨(sodium formate)에서 판정되었다(referenced).
High-Performance Liquid Chromatography/Tandem Mass Spectrometry (HPLC-MS/MS).

The Agilent 1100 Series HPLC system
- 구성
⇒ a pump, a degasser, and an autosampler (Agilent, Waldbronn, Germany) - a 4000 Q Trap triple quadrupole/linear ion trap mass spectrometer에 연결되었음.
(Applied Biosystems/MDS Sciex, Darmstadt, Germany) - -4500 V의 spray voltage으로 negative ionization mode로 작동하는
electrospray ionization (ESI) device를 장착. - 이 4극자들(quadrupoles)은
unit mass resolution에서 작동했음. - Nitrogen이 curtain gas (20 psi)로 작용했으며,
declustering potential은 ESI- mode에서 -10V ~ -85 V에서 설정되었음. - mass spectrometer는
음이온들을 모니터링하는 full scan mode에서 작동되었음. - 특정한 결과 이온들(product ions)로의 [M-H]- molecular ions의 분열(fragmentation)은
nitrogen (5×10-5 Torr)과의 충돌(collision)과
-15 to -70 V의 충돌에너지(collision energy)에 의해 유도되었음. - 분열 컨트롤과 데이터 획득을 위해,
the Sciex Analyst software (v1.4)가 사용되었음.
High-Performance Liquid Chromatography/Tandem Mass Spectrometry (HPLC-MS/MS).
- 커피 내의 bitter compounds 1-9a,b에 대한 HPLC-MS/MS analysis을 위해
an analytical 150mm×2.1mm i.d., 5 µm,
Zorbax Eclipse XDB C18 column (Agilent, Waldbronn, Germany)이 사용되었음. - 이 컬럼은 음이온들을 검출하는 the multiple reaction monitoring mode (MRM)에서 작동하는
mass spectrometer에 연결되었음. - 150 ms의 시간 동안에, the mass transitions
m/z 271→109 and 271→146이 compound 1과 2의 분석을 위해 사용되었고,
m/z 271→109 and 271→135가 compound 3의 분석,
m/z 273→109 and 273→135가 compound 4의 분석,
m/z 271→109 and 271→161이 compound 5와 6의 분석,
m/z 407→109 and 407→297이 compound 7과 8의 분석, 그리고
m/z 407→109 and 407→161이 ompounds 9a and 9b의 분석을 위해 사용되었다. - Nitrogen이 nebulizer gas (35 psi)으로서 그리고
solvent drying(45 psi)를 위한 turbo gas (350 ℃)로서 작용하였다. - 샘플의 주입(20 µL) 후에, chromatography가
flow rate of 250 µL/min으로 수행되었는데,
aqueous formic acid (0.1% in water)과 acetonitrile의 혼합물(75:25, v/v)로 시작하여,
5 min 내에 아세토니트릴(acetonitrile)의 함유율을 28%까지 증가시켰고,
그 다음 20 min 내에 30%까지, 그리고
그 다음 5 min 이내에 100%까지 증가시켰고,
마지막으로 추가적인 5 min 동안에는 함유율을 유지시키는 변율(gradient)을 사용하였다.
Nuclear Magnetic Resonance Spectroscopy (NMR).
- 핵자기공명분광분석법
- 1-D and 2-D NMR experiments이
a Bruker DMX-400 (Bruker, Rheinstetten, Germany)에서 수행되었다. - Chemical shifts는
the proton dimension의 internal standard로서 tetramethylsilane (TMS)를 사용하여
the carbon dimension에서의 d3-MeOD (49.3 ppm)의 carbon signal로부터 결정되었다.

RESULTS AND DISCUSSION
- 여러 raw coffee 성분들의 로스팅 중 bitter-tasting compounds 생성 잠재력을 평가하기 위한 목적으로,
5-O-caffeoylquinic acid, quinic acid, caffeic acid, ferulic acid, sucrose, 그리고 trigonelline이 각각
실험실 오븐에서 220 °C로 15 min 동안 분리되어 로스트 되었다. - Sucrose으로부터의 Maillard-type bitter compounds 생성에 대한 amino acids의 영향을 연구하기 위해,
추가적으로 raw coffee beans에 량적으로 지배적인 amino acids의 존재 하에 sucrose를 가열하였고,
아미노산들은 L-glutamic acid, L-proline, L-alanine, L-asparagine, and L-aspartate가 천연 농도 비율들로 사용되었다 [19]. - 로스트된 재료들은 cooling 후에, 온수에 넣어졌고, 상온에서 식힌 후에
개별적인 roasted precursor mixtures의 수용 추출물들이 수용액(pH 5.2)에서 관능평가되었고,
그것들의 쓴맛 강도(bitter taste intensities)가
0 (not bitter)에서 5(extremely bitter)까지의 5-point scale에서 채점되었다.

- Table 1에 주어진 결과들은
⇒ caffeic acid의 로스팅이 가장 강한 쓴맛을 내는 화합물을 만들었고,
strongly roasted, espresso-type coffee의 bitter quality를 연상시키는
very harsh type의 bitterness를 나타냈음을 보여주고 있다. - 또한 5-O-caffeoylquinic acid으로부터 형성된 반응산물들이
2.5점의 강도로 매겨진 평점으로 다소 강한 쓴맛을 나타냈다. - 5-O-caffeoylquinic acid 로스팅 산물들의 coffee-like bitter taste profile은
최근에 보고된 caffeoylquinic acid lactones의 bitter quality와 매우 가까웠다 [12]. - 비교할 때, trigonelline, sucrose, 그리고 sucrose/amino acid mixture의 열처리는 각각
0.5와 1.5 사이의 상당히 낮은 강도 점수를 가진 non-coffee-like bitter taste의 발달을 초래했다 (Table 1). - 흥미롭게도, quinic acid과 ferulic acid은
적용된 로스팅 조건 하에서 어떠한 쓴 화합물들을 각각 생성하지 않았다 (Table 1).
Taste Dilution Analysis of Thermal Degradation Products of Caffeic Acid.
- Caffeic acid으로부터 형성된
intensely harsh bitter-tasting compounds의 특징분석을 목적으로,
⇒ 220~500nm 범위의 wavelength에서 작동하는
a diode array detector에 연결된 RP-HPLC를 이용하여
hydrophobic reaction products을 분리해내었다. - Figure 1에 나타난 바와 같이, 엄청난 다양성의 반응산물들이 검출될 수 있었다.
- 맛 활성이 덜하거나 없는 물질들로부터 strongly bitter compounds을 가려내기 위하여,
우리는 먼저 최근에 개발된 taste dilution analysis [12-17]을 적용하여
이 반응산물들을 스크린하였다. - 이를 위해,
⇒ HPLC separation의 effluent가 24 fractions로 수거되었고 (Figure 1),
⇒ RP-18 cartridges를 사용하여 solid phase extraction에 의하여
taste compounds가 정제되었다. - 그 분리해낸 화합물들을 동일한 양의 병입 된 물 (pH 5.2)에 넣었고
⇒ 그 다음에 각 fraction이 water (pH 5.2)로
단계별로 1:1 희석되었으며(stepwise diluted 1:1)
⇒ 훈련된 센서리 패널에게 농도가 높아지는 순서로 제시되었다. - 패널리스트들에게 taste quality를 평가하도록 요구했고
triangle test에 의해 detection threshold를 결정하도록 하였다. - high TD-factors로 나타난 바와 같이
⇒ HPLC fractions 10과 14가 highest bitter impacts를 가진 것으로 평가되었고
⇒ 바로 그 다음이 fractions 11-13, 15, 17, 19- 21, 24이었다 (Figure 1). - 다른 모든 fractions는
⇒ 어느 정도 낮은 taste impacts를 가지거나 혹은 전혀 tasteless한 것으로 평가되었다. - 이어지는 식별 실험들은
HPLC fractions 10-15, 17, 20, and 21 내의 bitter compounds에 초점을 맞추었다.
Structure Determination of Bitter Compounds.
- Fractions 10-15, 17, 20, and 21에서 강렬한 쓴맛 감각을 부여하는 분자들에 대한 첫 통찰을 얻기 위해,
⇒ 개별 taste compounds을 semipreparative RP-HPLC에 의하여 분리했고,
⇒ 그들의 화학구조들을
UV/vis,
LC-MS/MS와
1-D/2-D NMR experiments으로 해명하였다(elucidate). - HPLC fractions 11 and 12에서 분리되어진 1과 2의 UV/vis spectra는
⇒ 286 nm에서 동일한 absorption maximum을 보인 반면,
HPLC fraction 13으로부터 얻어진 taste compound 3은
⇒ 263 and 283 nm에서 2개의 absorption maxima를 나타냈다. - 추가적으로, LC-MS analysis는 1과 3의 경우에
⇒ 강한 유사분자 이온(intense pseudo-molecular ion) [M-H]- with m/z 271를 나타냈다. - ┌ 1H NMR spectroscopy에 의해 얻어진 데이터에 대한 분석 뿐만 아니라,
├ homonuclear (gs-COSY)와
│ heteronuclear 2-D NMR experiments (HMQC and HMBC) 그리고
└ 문헌[20, 21]에서 caffeic acid 분해산물에 대해 보고된 것들과 비교한 결과,
다음 세 가지로서 HPLC fractions 11-13에서 bitter compounds의 명백한 식별을 할 수 있었다.
■ trans-5,6-dihydroxy-1-methyl-3-(3′,4′-dihydroxyphenyl) indane (1),
■ cis-5,6-dihydroxy-1-methyl3-(3′,4′-dihydroxyphenyl) indane (2),
■ trans-1,3-bis(3′,4′- dihydroxyphenyl)-1-butene (3) (Figure 2). - 비록 이 화합물들이 heat treatment 중에 caffeic acid로부터 방출된
4-vinylcatechol의 condensation products로 선행연구에서 보고된 바 있지만 [20, 21],
이 분자들의 bitter taste activity는 지금까지 보고된 적이 없다. - HPLC fraction 14로부터 분리해낸 bitter compound 4 에 대한 LC-MS analysis는
⇒ ESI- mode에서 m/z 273를 가진 유사 분자 이온(pseudo-molecular ion)을 나타냈고,
⇒ 이는 1-3에 비교할 때 2개의 추가적인 그 분자 내 양성자(two additional protons)를 가리키는 것이다. - 1H NMR spectrum은 10개의 resonance signals을 보였다.
⇒ 3개의 양성자들의 통합된 1개의 시그날,
2개의 양성자들의 2개의 시그날, 그리고
1개의 양성자 만에 대한 7개의 시그날 - 6.4 and 6.7 ppm 사이의 화학적 이동 범위에서,
4-substituted 1,2-dihydroxybenzene moiety의 전형적인 커플링 패턴이 두 번 관찰되었다. - 또한 그 gs-COSY spectrum은
┌ 1.75 ppm에서 공명하는(resonating) methylene protons H-C(2)과
└ protons H-C(1) and H-C(3) 사이에서의 강한 커플링(strong couplings)을 보였다. - 나아가, proton H-C(1)이 methyl protons H-C(8)과의 homonuclear connectivity을 보였고, 그리고
그것의 downfield shift으로 인하여 C(1)은 4-position에서
1,2-dihydroxybenzene moieties 중 하나에 연결되어있을 것이다. - H-C(3)은 H-C(2)와만 coupling을 보였고,
H-C(1)의 경우에 관찰된 것과 비슷한 downfield shift가 발견되었으므로,
methylene group C(3)는 두번째 1,2-dihydroxybenzene system에 링크되어야 한다. - 이런 발견들은
2JC,H와 3JC,H coupling constants에 최적화된
heteronuclear multiple bond correlation spectroscopy (HMBC)와
1JC,H coupling constants에 적합한
heteronuclear multiple bond correlation spectroscopy (HMBC)에 의해 더 강화되었다. - HMBC 실험은
methylene group H-C(3)와 adjacent carbon atoms C(2)과 C(1′) 뿐만 아니라
aromatic carbons C(2′)와 C(6′) 간의 correlations를 나타냈고,
따라서 Figure 2에서 제안된 구조를 입증(corroborating)한다. - 또한, H-C(1)과 carbon atoms C(8), C(2), C(3) 간의 long-range correlations와
aromatic carbons C(1a), C(3a), and C(7)로의 coupling이
C(1)과 and the second 1,2-dihydroxybenzene moiety 간의 connection을 가시화하였다. - 모든 스펙트로스코픽 데이터를 감안할 때,
HPLC fraction 14에서 분리되어진 bitter compound는
⇒ 선행연구에서 보고되지 않은
1,3-bis(3′,4′-dihydroxyphenyl) butane (4) (Figure 2)으로 식별될 수 있었다. - HPLC fraction 15로부터 분리해낸 bitter compound 5 에 대한 LC-MS analysis는
⇒ 1-3의 경우에 발견된 것과 동일한 [M-H]– ion m/z 271을 나타냈다.
⇒ 또한, 5의 UV/vis spectrum은 1과 2의 경우에 얻어진 스펙트럼과 같았다. - Compound 5의 1-D/2-D NMR 데이터를 tastant 1의 경우에 얻어진 것과 비교하니
어느 정도 주요한 유사성들을 나타냈다. - gs-COSY experiment는
carbon skeleton C(8)/C(1)/C(2)/C(3)의 protons의 경우에 coupling pattern이
compound 1의 경우에 관찰된 것과 동일한 패턴을 보였다. - 그러나, 1,2-dihydroxybenzene substituents 중 하나의 coupling pattern은
1과 5의 NMR data에서 주요한 차이를 보였다. - 2개의 싱글릿들(singlets=단일선=원자의 단일항 간의 천이에 의해 생기는 스펙트럼선)이
1에 있는 phenylindane system의 two aromatic protons H-C(4)와 H-C(7)의 경우에 검출될 수 있었지만,
2에 있는 phenylindane structure의 protons H-C(6)과 H-C(7)은
인근 양성자들(vicinal protons)에게 기대되는
two doublets with a coupling constant of 7.8 Hz으로 관찰되었다. - 이런 coupling pattern은
phenylindane의 five-membered carbocycle(5원 탄소고리)가
α- and β-positions에서 C(4)에 붙어 있다는 것을 가리킨다. - 모든 NMR 데이터를 주의 깊게 고려해볼 때,
HPLC fraction 15로부터 분리되어진 bitter compound 5는
⇒ 앞서 보고된 적이 없는
⇒ trans-4,5-dihydroxy-1-methyl-3-(3′,4′- dihydroxyphenyl) indane (5) (Figure 2)인
것으로 식별될 수 있었다. - LC-MS (ESI–) analysis of 7 isolated from HPLC fraction 20
⇒ 유사분자 이온(pseudo-molecular ion) [M–H]– with m/z 407을 나타냈다. - LC-MS/MS 실험들은
⇒ a daughter ion with m/z 297를 나타냈는데,
⇒ 아마 pyrocatechol moiety의 loss에 상응하는 것일 것이며
⇒ a pyrocatechol ion을 나타내는 a daughter ion with m/z 109를 나타냈다. - 또한 7은
⇒ 1, 2, 5, and 6과 거의 동일한 UV/vis spectrum을 각각 보였고,
⇒ 따라서 7도 역시 a phenylindane structure를 보인다는 강한 증거를 제공하는 것이었다. - 1H NMR spectrum은
⇒ phenylindanes 1, 2, 5, and 6에 비해,
1개의 추가적인 methyl and methine group 그리고
2개의 추가적인 aromatic protons를 가진
총 14개의 14 resonance signals를 보였다. - protons H-C(8), H-C(1), H-C(2α), H-C(2β), and H-C(3)과
그들의 chemical shifts는
⇒ 1의 경우에 관찰된 것과 거의 동일했다. - 또한, 1에서 para-configured aromatic protons H-C(4) and H-C(7)이
7의 NMR spectrum 에서 6.37 and 6.62 ppm에서 검출될 수 있었으며,
⇒ 이는 그 분자 내에서의 1의 phenylindane structure를 확인해주는 것이다. - the phenylindane structure의 C(3)에 붙은 dihydroxybenzene residue는, 1과 반대로
⇒ long-range coupling (2 Hz)을 가진 단 2개의 aromatic protons H-C(2′) and H-C(6′) 만을 보였다. - 이 관찰된 long-range coupling constant는
다른 substituent가 position C(5′)에 연결되었을 때 볼 수 있다. - 이 가정은
C(5′)과 그리고 1.47 and 4.36 ppm에서 각각 resonating하는 추가적인 methyl and methine protons 간의
heteronuclear coupling을 보여주는 HMBC 실험들에 의해 강화될 수 있었다. - 후자의 시그날들은
7.2 Hz의 coupling constant를 가진 a duplet and a quartet으로 나타났으며,
133.3 and 138.1 ppm에서 resonating하는 네 번째(quaternary) 탄소원자들 C(5′) and C(2′′)로의
coupling을 보였다. - H-C(1′′)과 aromatic protons H-C(6′) and H-C(7′′) 간의 추가적인 연결(connectivity)이
⇒ HPLC fraction 20에서 분리된 화합물의 구조를
⇒ 앞서서는 보고된 적이 없는
trans-5,6-dihydroxy-1-methyl-3-[3′,4′- dihydroxy-5′-(1-(3′′,4′′-dihydroxyphenyl)-1-ethyl)phenyl] indane (7) (Figure 2)로 확인해주었다. - HPLC fraction 21로부터 얻어진 taste compound 8.
- 이것도 역시 [M-H]– ion with m/z 407을 나타냈고
Compound 7의 경우에 발견된 것과 같은
MS/MS fragmentation pattern과
a proton NMR spectrum with 14 resonance signals를 보였다. - phenylindane moiety의 chemical shifts와 coupling pattern은
2의 경우에 발견된 것과 비슷했으나,
aromatic protons인 methyl protons과 methine proton의 추가적인 시그날들은 7의 경우와 비슷했다. - 모든 NMR 데이터에 대한 신중한 고려를 통하여
HPLC fraction 21에서 분리해낸 taste compound를
⇒ 선행 연구에서 보고된 적이 없는 다음과 같은 것으로
명백하게 부여할 수 있었다.
⇒ cis-5,6-dihydroxy-1-methyl-3- [3′,4′-dihydroxy-5′-(1-(3′′,4′′-dihydroxyphenyl)-1-ethyl)phenyl] indane (8)
(Figure 2). - Bitter compound 9a isolated from HPLC fraction 10
- 9a는
⇒ LC-MS spectrum에서 quasi-molecular ion with m/z 407을 보였고
⇒ 1H NMR spectrum에서는 7과 8에서 이미 발견된 바와 같이
총 14개의 resonance signals를 보였다.
⇒ 또한 aliphatic protons의 chemical shifts와 coupling topology 역시
7과 8의 phenylindane structure와 일치적이었다. - 9a는
⇒ 이 taste compounds들과는 대조적으로
⇒ the phenylindane system의 carbon C(2)에 연결된
1-(3,4-dihydroxyphenyl)-1-ethyl residue를 보였다. - 이것은 H-C(2)와 H-C(1) 사이 뿐만 아니라
H-C(1′′) 사이의 homonuclear couplings을 보이는
gs-COSY spectrum으로부터 얻어진 데이터와,
이들 methine protons와 adjacent methyl groups C(8) and C(8′′) 사이의 correlations에 의해서
강화되었다. - 또한, 2,3J coupling constants에 최적화된 heteronuclear correlations이
⇒ H-C(1′′) and H-C(8′′) with the quaternary carbon atom C(2′′)의 coupling을 나타냈고
⇒ 그리고 H-C(2) with C(1′′) 사이의 correlations을 나타내어
⇒ the phenylindane system의 position 2로의
the 1-(3,4- dihydroxyphenyl)-1-ethyl residue의 부착(attachment)을 확인해준다. - 모든 스펙트로스코픽 데이터를 고려할 때,
HPLC fraction 10에서 분리되어진 bitter compound 9a는
⇒ 문헌상에 보고된 적이 없는
5,6-dhydroxy-1-methyl-2-[1-(3′,4′-dihydroxyphenyl)-1-ethyl]-3-(3′′,4′′-dihydroxyphenyl) indane
(Figure 2)로 식별될 수 있었다. - Fraction 10으로부터 9b도 분리되어질 수 있었는데,
⇒ 9a와 동일한 LC-MS and UV/vis spectrum 그리고 유사한 NMR data를 보이고 있으며,
⇒ 따라서 taste compound 9a의 diastereomer의 존재를 가리키고 있다. - 불행하게도, 얻어진 spectroscopic data는
bitter compounds 9a and 9b의 exact stereochemistry의 더 정확한 부여를 가능케하지는 못했다.
Bitter Recognition Threshold Concentrations.
- 센서리 분석 이전에, taste compounds 1-9a,b까지의 purity가
HPLC-MS 뿐만 아니라 1H NMR spectroscopy에 의해 체크되었다. - 쓴맛에 대한 사람의 식역 농도를 결정하기 위하여,
1-9a,b의 수용액 (pH 5.2)이 triangle test에 의해 평가되었다 (Table 2). - 그 구조와 독립적으로,
모든 화합물들은 23~178 µmol/L에 이르는 threshold concentrations로 쓴맛을 부여했다. - 45 µmol/L 미만의 값을 가진 최저 식역들이 4-6와 9a,b의 경우에 발견된 반면,
phenylindane 1은 178 µmol/L의 최고 식역 농도를 보였다 (Table 2). - 게다가, 센서리 패널들은
이 페놀 화합물들의 taste profile가
최근에 식별된 caffeoyl quinides [12]의 bitter quality와 유의하게 다른 것으로 평가했다. - caffeoyl quinides는 a pleasant coffee-like bitter taste를 가진 것으로 평가된 반면 [12],
1-9a는 a strongly roasted, espresso-type coffee의 bitter quality를 연상시키는
a more harsh bitter taste를 나타냈다.

Identification of Bitter Compounds 1-9a,b in Coffee Brew.
- 커피 음료 내의 caffeic acid derived bitter compounds의 존재를 검증하기 위하여
- the multiple reaction monitoring (MRM) mode에서 작동하는
LC-MS/MS (ESI-)를 이용하여
a freshly prepared coffee brew를 이 화합물들에 대해 스크린 하였다. - 분석 이전에, tuning runs에서 각 맛 화합물들에 대해 characteristic mass transitions이 선택되었다.
- 그런 다음, 커피 내 맛 화합물들의 characteristic mass transitions 뿐만 아니라
retention time이 레퍼런스 화합물들의 것들과 비교되었다. - Figure 3에 보여진 바와 같이,
target compounds 1-9a,b 각각에 1개의 mass transition의 경우에,
이들 caffeic acid derived bitter compounds 각각이
coffee brew에서 HPLC-MS/MS (MRM)에 의해 검출될 수 있었다. - 또한, 커피 내의 그 bitter tastants 1-9a,b의 정체가
상응 레퍼런스 화합물들과의 co-chromatography에 의해서 확인되었다. - 우리가 아는 바로는, 이 bitter compounds는 문헌상에서 커피 음료 내의 쓴맛 물질로 보고된 적이 없었다.

Formation Pathways of Bitter Compounds 1-9a,b.
- free caffeic acid (유리 카페산)이 커피 내에 다소 소량으로 존재하는 것으로 알려져 있기 때문에,
bound caffeic acid (결합 카페산) 예를 들어,
⇒ 5-O-caffeoylquinic acid는
로스팅 중에 쓴 화합물 1-9a,b를 생성할 수 있을 것이다. - 이 가정을 체크하기 위해,
⇒ 5-O-caffeoylquinic acid를 모델 실험에서 열처리하였고,
⇒ 형성된 로스팅 산물들에 대해
MRM mode에서 작동하는 LC-MS/MS에 의해 bitter tastants 1-9a,b를 분석하였다. - Figure 4에 나타난 바와 같이,
⇒ 모든 쓴 화합물들이
⇒ 그들의 retention times, mass transitions, 그리고 상응하는 레퍼런스 화합물들과의
cochromatography에 기초하여 식별되었다. - 이 결과들은,
⇒ bitter compounds 1-9a,b 형성의 precursor로서
커피의 주요 페놀인 5-O-caffeoylquinic acid을 명확하게 보여준다.


- Figure 5에 이 발견 결과에 기초하여,
5-O-caffeoylquinic acid의 열분해로부터
bitter taste compounds 1-9로 이끄는 반응 경로 맵이 개관되어 있다. - 5-O-Caffeoylquinic acid (1)은
가수분해로 caffeic acid (2)를 방출시킬 수 있고
그것은 탈카르복실화(decarboxylation) 중에,
고-반응성의 4-vinylcatechol, 3a를 생성하는 것으로 보고된 바 있다 [20-22]. - 그렇지 않으면,
5-O-Caffeoylquinic acid (1)의 thermal syn-elimination이
4-vinylcatechol (3a)을 직접 유발할 수 있을지도 모른다. - 그 vinyl function에서 3a의 Protonation이
the electrophile(친전자체) 3b를 초래하는데,
그것은 the nucleophile(친핵체) 3a와 dimerize(이량화)할 수 있고
그래서 핵심 중간물질인 4를 유발할 수 있는 것이다. - 그러면 oxonium ion(옥소늄 이온) 4가
예를 들어, 1과 1의 분자 1개의 1,2-dihydroxybenzene moiety과의
산화환원반응(redox reaction)에 의하여
bitter compound 4로 줄어들 수 있거나, 또는
rearomatization(재-아로마화) 중에 bitter compound 3를 생성할 수 있다. - 그렇지 않으면, 그 옥소늄 이온의 unsaturated Michael system과
다른 1,2-dihydroxybenzene moiety의 ortho-positions 중 하나 사이의
intramolecular ring-closure reaction이
각각 phenylindanes 1, 2, 5, and 6을 각각 유발한다. - 이들 쓴맛 나는 4-vinylcatechol dimers로부터 시작하여,
trimers 7, 8, and 9a,b의 형성이 쉽게 설명가능하다. - 화합물 3과 the vinylcatechol oxonium ion (3b)의 다른 분자와의 축합(condensation)이
ring-closure 중에 phenylindane 9a,b로 이끄는 반면,
phenylindanes 1 and 2와 3b와의 반응이 4-vinylcatechol trimers 7 and 8를 유발한다.
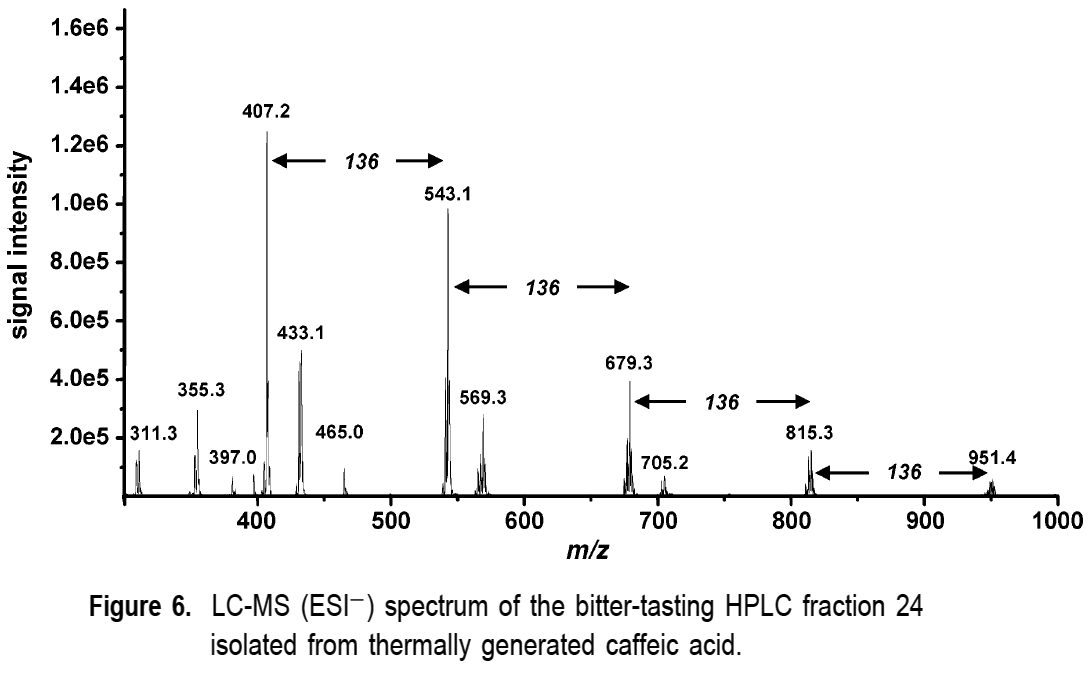
LC-MS Studies on the Bitter-Tasting HPLC Fraction 24.
- 앞서 식별된 쓴맛 화합물들 이외에,
HPLC fraction 24도 bitterness에 대한 높은 TD-factor를 가지는 것으로 평가되었다 (Figure 1). - 그러나, 그 복잡한 플랙션 내의 개별 쓴맛 화합물들을 분리해내어 더 정제하는 어떠한 시도도 이제까지 성공하지 못했다.
- 그 플랙션 내의 쓴 화합물의 화학적 성격에 대한 더 일반적인 통찰들을 얻기 위해,
the total HPLC fraction 24가 LC-MS (ESI-) 스터디들에 사용되었다. - Figure 6에 주어진 바와 같이,
그 MS spectrum은
bitter-tasting trimers 7-9a,b의 경우에 발견된 pseudo-molecular와
잘 들어맞는 m/z 407를 가진 지배적인 이온을 보였고,
따라서 추가적인 4-vinylcatechol trimers의 존재를 가리키고 있다. - 또한, m/z 543, 679, 815, and 951의 pseudo-molecular ions(유사 분자 이온들)가
mass spectrum에서 관찰되었다. - 이 이온들은
dimers(2분자체)와 trimers(3분자체) 이외에,
적어도 heptamer(7량체)까지의 higher 4-vinylcatechol oligomers가
각각 caffeic acid와 caffeoylquinic acids로부터 나온
4-vinylcatechol의 protoncatalyzed oligomerization에 의하여
로스팅 중에 형성된다는 것을 가리킨다. - The higher 4-vinylcatechol oligomers의 정확한 분자 구조에 관한 스터디와
그들의 센서리 활성도, 그리고 이 4-vinylcatechol에서 도출된 반응산물들이 커피의 bitterness에 미치는 공헌에 관한 스터디가 현재 진행 중이다.

LITERATURE CITED
(1) Semmelroch, P.; Grosch, W.
Analysis of roasted coffee powders and brews by gas chromatography-olfactometry of headspace samples.
Lebensm.-Wiss. Technol. 1995, 28, 310-313.
(2) Semmelroch, P.; Grosch, W.
Studies on character impact odorants of coffee brews. J. Agric. Food Chem. 1996, 44, 537-543.
(3) Mayer, F.; Czerny, M.; Grosch, W.
Sensory study of the character impact aroma compounds of a coffee beverage.
Eur. Food Res. Technol. 2000, 211, 272-276.
(4) Chen, W. C.
Studies on the bitter taste of roasted coffee. Relationship between structure and bitter taste of
some organic compounds (in German).
Ph.D. Thesis, University of Munich, Munich, Germany, 1979.
(5) Shibamoto, T.; Harada, K.; Mihara, J.; Nishimura, K.; Yamaguchi, A.; Aitoku, A.; Fukada, T.
Application of HPLC for evaluation of coffee flavor quality.
In The quality of foods and beVerages, Vol. 2; Charambous, G., Inglett, G., Eds.;
Academic Press, New York, 1981; p 311.
(6) Belitz, H. D. Taste Active substances in coffee; ASIC 7th Colloquium: Hamburg, Germany, 1977; pp 243-252.
(7) Ginz, M.; Engelhardt, U. H.
Identification of praline-based diketopiperazines in roasted coffee.
J. Agric. Food Chem. 2000, 48, 3528-3532.
(8) Rizzi, G. P.; Boekley, L. J.; Ekanayake, A.
The influence of roasting derived polymeric substances on the bitter taste of coffee brew.
In Nutraceutical Beveragess Chemistry, Nutrition, and Health Effects; Shahidi, F., Weerasinghe, D. K., Eds.;
ACS Symposium Series 871: Washington DC, 2004; pp 229-236.
(9) Ginz, M.; Engelhardt, U. H.
Analysis of bitter fractions of roasted coffee by LC-ESI-MS-New chlorogenic acid deriVatiVes.
Proceedings of the 19th ASIC Symposium: Trieste, Italy, 2001; pp 248-252.
(10) Maga, J. A.
Simple phenol and phenolic compounds in food flavor. CRC Crit. ReV. Food Sci. Nutr. 1978, 10, 323-372.
(11) McCamey, D. A.; Thorpe, T. M.; McCarthy, J. P.
Bitterness in Foods and Beverages.
In DeVelopments in Food Science; Rouseff, R. L., Ed.; Elsevier Science Publishers: Amsterdam, 1990; pp 169-182.
(12) Frank, O.; Zehentbauer, G.; Hofmann, T.
Bioresponse guided decomposition of roast coffee beverage and identification of key bitter-tasting compounds.
Eur. Food Res. Technol. 2006, 222, 492-508
(13) Frank, O.; Hofmann, T.
Characterization of an intense bitter-tasting 1H,4H-quinolizinium-7-olate
by application of the taste dilution analysis, a novel bioassay for screening and identification
of taste active compounds in foods.
J. Agric. Food Chem. 2001, 49, 231-238.
(14) Ottinger, H.; Bareth, A.; Hofmann, T.
Characterization of natural cooling compounds formed from glucose and L-proline in dark malt by application of the taste dilution analysis. J. Agric. Food Chem. 2001, 49, 1336-1344.
(15) Czepa, A.; Hofmann, T.
Structural and sensory characterization of compounds contributing to the bitter off-taste of carrots (Daucus carota L.) and carrot puree.
J. Agric. Food Chem. 2003, 51, 3865-3873.
(16) Ottinger, H.; Hofmann, T.
Identification of the taste enhancer alapyridaine in beef broth and evaluation of
its sensory impact by taste reconstitution experiments. J. Agric. Food Chem. 2003, 51, 6791-6796.
(17) Scharbert, S.; Holzmann, N.; Hofmann, T.
Identification of the astringent taste compounds in black tea infusions by combining
instrumental analysis and human bioresponse. J. Agric. Food Chem. 2004, 52, 3498-3508.
(18) Wieser, H.; Belitz, H.-D.
Studies on the structure/activity relationship of bitter-tasting amino acids and peptides (in German).
Z. Lebensm.-Unters.-Forsch. 1975, 159, 65-72.
(19) Müller, C.; Hofmann, T.
Screening of raw coffee for thiol binding site precursors using in bean model roasting experiments.
J. Agric. Food Chem. 2005, 53, 2623-2629.
(20) Stadler, R.; Welti, H.- D.; Stämpfli, A.; Fay, L.
Thermal decomposition of caffeic acid in model systems: Identification of
novel tetraoxygenated phenylindan isomers and their stability in aqueous solution.
J. Agric. Food Chem. 1996, 44, 898-905.
(21) Rizzi, G.; Boekley, L.
Observation of ether-linked phenolic products during thermal degradation of ferulic acid in the presence of alcohols.
J. Agric. Food Chem. 1992, 40, 1666- 1670.
(22) Scholtzhauer, W. S.; Snook, M. E.; Chortyk, O. T.; Wilson, R. L.
Pyrolytic evaluation of low chlorogenic acid tobaccos in the formation of the tobacco smoke co-carcinogen catechol.
J. Anal. Appl. Pyrolysis 1992, 22, 231-238.
- The end -