커피의 쓴맛을 증진하는 화합물들

| ■ Abstract | |
| 1. Introduction | |
| 2. Materials and Methods | |
| 2.1 Chemicals | |
| 2.2 Coffee beans | |
| 2.3 Coffee brew sample preparation | |
| 2.4 Coffee green bean roasting preparation |
|
| 2.5 Bitter intensity evaluation of coffee brew |
|
| 2.6 UPLC/MS chemical profiling | |
| 2.7 Multivariate statistical analysis (MVA) |
|
| 2.8 Off-line Multidimensional preparative-liquid chromatography/mass spectrometry (Prep-LC/MS) fractionation |
|
| 2.9 Quantification by ultra-performance liquid chromatography–tandem mass spectrometry (UPLC–MS/MS) |
|
| 2.10 Sensory recombination analysis | |
| 2.11 Consensus sensory analysis of individual compounds | |
| 2.12 Nuclear magnetic resonance |
|
| 2.13 Data analysis | |
| 3. Results | |
| 3.1 Multivariate statistical modeling | |
| 3.2 Isolation and identification of positively correlated compounds |
|
| 3.3 Quantification of positively correlated compounds | |
| 3.4 Sensory recombination analysis of positively correlated compounds | |
| 3.5 Impact of roasting on the generation of compounds 1–5 |
|
| 4. Conclusions | |
| ■ Appendix A Supplementary data |
|
| ■ References |
|

Abstract
- 커피의 쓴맛 지각은 소비자 수용에 영향을 미치는 핵심적인 속성 중 하나이다.
- Nontargeted liquid chromatography/mass spectrometry (LC/MS) flavoromics analysis를 통해
로스팅된 커피 브루의 쓴맛 지각을 향상시키는 화합물들을 식별했다. - Orthogonal partial least squares (OPLS) analysis를 사용하여
14가지 커피 브루들의 포괄적인 화학적 프로파일들과 센서리 쓴맛 강도 평점들을 모델링했으며,
적합도와 예측성이 우수했다. - OPLS 모델에서 예측성이 높고 쓴맛 강도와 양의 상관관계가 있는 5가지 화합물을 선별하고,
preparative LC fractionation (분취용 LC 분획법)을 사용하여 추가로 분리 및 정제했다. - Sensory recombination testing (관능적 재조합 시험) 결과,
5가지 화합물은 혼합물로 제공되었을 때 커피의 쓴맛 지각을 유의미하게 향상시켰지만,
개별적으로 제공되었을 때는 그렇지 않은 것으로 나타났다. - 또한, 일단의 로스팅 실험을 통해 이 5가지 화합물이 커피 로스팅 과정에서 생성되었음을 확인했다.
1. Introduction
- 커피는 전 세계적으로 가장 널리 소비되는 음료 중 하나로, 2014년 이후 연평균 2.1%의 성장률을 보이고 있다 (ICO, 2019).
- 커피 특유의 플레이버와 자극적인 효과는 소비 행동에 영향을 미치는 중요한 속성으로 여겨진다 (Nehlig et al., 1992).
- 역사적으로 커피 플레이버 연구는 주로 아로마에 집중되어 왔으며, 800개 이상의 휘발성 화합물이 확인되었다
(Blank et al., 1991; Nijssen, 1996; Semmelroch & Grosch, 1996; Semmelroch et al., 1995). - 이와는 대조적으로, 커피의 맛, 특히 특유의 쓴맛을 담당하는 화합물은 잘 알려져 있지 않다.
- 현재 커피에서 약 30종의 쓴맛 화합물이 확인되었다.
- 잘 알려진 쓴맛 화합물인 카페인은 커피 쓴맛의 30%만을 차지하는 것으로 알려져 있다 (Chen, 1979).
- 커피에서 보고된 다른 쓴맛 화합물로는
■ proline-based 2,5-diketopiperazines (프롤린 기반 2,5-디케토피페라진)
(Ginz and Engelhardt, 2000; Stark and Hofmann, 2005)과
■ 로스팅 과정에서 생성되는 것으로 알려진
furfuryl alcohol (푸르푸릴알코올),
5-hydroxymethyl-2-furanaldehyde (5-하이드록시메틸-2-푸란알데히드),
pyrazines (피라진류)와 같은 헤테로고리 화합물이 있다.
(Belitz, 1977; Shibamoto et al., 2012) - Frank, Zehentbauer, and Hofmann (2006)은
쓴맛 식역치가 9.8~180 μmol/L인, 약배전에서 중배전 커피에서
■ caffeoyl quinides (카페욜 퀴나이드),
■ dicaffeoyl quinides (디카페욜 퀴나이드), 그리고
■ feruloyl quinides (페룰욜 퀴나이드)의 열적으로 생성된 여러 구조 이성질체를 확인했다. - 또한, 더 높은 로스팅 온도에서
caffeoyl quinides와 feruloyl quinides가 더욱 분해되면
다크 로스팅 커피에서
■ 4-vinylcatechol oligomers (4-비닐카테콜 올리고머)와 같은
쓴맛 화합물이 생성되는 것으로 나타났다
(Frank, Blumberg, Kunert, Zehentbauer, & Hofmann, 2007). - 더 나아가, Kreppenhofer, Frank, 그리고 Hofmann(2011)은
커피에서 100~537 μmol/L의 비교적 높은 쓴맛 식역치를 가진 새로운 종류의 쓴맛 화합물인
■ hydroxylated phenylindanes (수산화 페닐인단) 계열을 확인했다. - 최근에는
■ 푸로카우란 배당체(furokaurane glucoside)인 mozambioside (모잠바이오사이드)가
아라비카 커피에서 특별히 쓴맛을 내는 화합물로 확인되었으며,
쓴맛 식역치는 60μmol/L이다 (Lang, Klade, Beusch, Dunkel, & Hofmann, 2015). - 역사적으로, 테이스트 디스커버리를 위한 분석적 방법은 주로 센서리-유도 분획(sensory-guided fractionation) 기법과 식역 값(threshold values)을 결합하여 어떤 화합물이 플레이버 반응에 기여하는지 파악해 왔다.
- 그러나 센서리 식역치 이상에서 보고된 개별 쓴맛 화합물의 합으로 커피의 쓴맛 지각을 완전히 설명하는 것은 지나치게 단순화된 설명일 가능성이 높다.
- 맛 수용체는 복잡한 화합물(리간드) 상호작용의 영향을 받는 것으로 알려져 있다 (Breslin and Beauchamp, 1995, Calvino et al., 1990, Stevens, 1997).
- 예를 들어, 역치 이하 레벨에서 화합물들은 플레이버 지각(perception)에 상당한 영향을 미치는 것으로 나타났다(Dalton et al., 2000, Delwiche and Heffelfinger, 2005, Miyazawa et al., 2008, Saison et al., 2009, Sterckx et al., 2011).
- Lioe, Apriyantono, Takara, Wada, and Yasuda (2005)는
식역 이하 농도에서 L-Phenylalanine (페닐알라닌)이 간장(soy sauce) 그리고, 글루탐산나트륨(MSG)과 염화나트륨(NaCl) 혼합 용액의 감칠맛(umami taste)을 유의미하게 향상시킬 수 있음을 발견했다.
그러나 MSG 단독의 감칠맛(umami taste)은 L-Phenylalanine에 의해 향상되지 않았다. - 따라서 커피의 쓴맛 지각 또한 복잡한 화합물 상호작용의 영향을 받을 것으로 예상된다.
- 최근, 화합물 상호작용을 조사하는 플레이버 디스커버리의 방법이 도입되었는데,
이 방법은 화학계량학을 적용하여
관심 속성의 감각 지각에 대한
식품의 非標的 종합적인 화학적 프로파일(nontargeted comprehensive chemical profiles)을 모델링한다. - 이 접근법은
식품의 모든 화합물들을, 직접적으로 맛-활성적인 것들이 아니라
오히려 플레이버 지각에 대한 잠재적 기여자로 간주한다
(Charve et al., 2011, Gao et al., 2021, Ronningen et al., 2017, Sittipod et al., 2019, Sittipod et al., 2020). - 이 접근법은
개별적으로는 뚜렷한 플레이버를 나타내지 않지만,
복잡한 식품이나 모델 시스템에서 플레이버 프로파일에 영향을 미치는 화합물의 발견으로 이어졌다. - Sittipod et al., 2019, Sittipod et al. (2020)은
커피의 플레이버 품질을 크게 변화시키는 새로운 클로로겐산 파생물들(chlorogenic acid derivatives)과
ent-kaurane diterpenes를 발견했다. - 더 최근에는 Gao et al. (2021)은 커피에서 쓴맛 知覺을 억제하는 세 가지 화합물을 확인했다.
- 이러한 결과는 식품 샘플의 복잡한 플레이버 知覺에 공헌하는 화합물을 이해하는 데 있어 非標的 香味體學 接近法(nontargeted flavoromics approach)의 가치를 보여준다.
- 본 연구의 주요 목표는
■ 커피 쓴맛 지각를 향상시키는 화합물을 규명하기 위해 비표적 플레이버로믹스 접근법을 적용하는 것이었다.
■ 다변량 통계 분석을 적용하여 쓴맛 강도 평점들로 14가지 커피의 화학적 프로파일을 모델링했다.
■ 이후, 예측성이 높은 양의 상관관계를 가진 화합물들을 선별하고,
■ preparative Liquid Chromatography/Mass Spectrometry (LC/MS)로 추가 분리한 후,
■ Ultra Performance Liquid Chromatography/Mass Spectrometry-Quadruple time of flight
(UPLC/MS-QToF)과 nuclear magnetic resonance (NMR)로 동정했다.
■ 또한, sensory recombination analysis (감각 재조합 분석)을 통해
감각적 영향(sensory impact)을 검증했다.
2. Materials and Methods
2.1 Chemicals
- UPLC급 포름산(formic acid), 아세토니트릴(acetonitrile), 아세톤(acetone), 메탄올(methanol), 일염기성 인산나트륨(monobasic sodium phosphate), 이염기성 인산나트륨(dibasic sodium phosphate), 염산 (hydrochloric acid)(HCl)은 Fisher Scientific (Waltham, MA)에서 구입했다.
- 카페인(Caffeine), 메틸파라벤(methylparaben), 중수소화 메탄올-d4(deuterated methanol-d4), 디메틸 설폭사이드-d6(dimethyl sulfoxide-d6)는 Millipore Sigma (Burlington, MA)에서 구입했다.
- 나노퓨어 워터 여과에는 Barnstead nano91 diamond system (Thermo Fisher, Waltham, MA)을 사용했다.
- 류신 엔케팔린(Leucine enkephalin)과 Oasis HLB 카트리지 (10mg 및 6g)는 Waters Co.(Milford, MA)에서 구입했다.
2.2 Coffee beans
- 7개 제조업체에서 생산된 총 14가지의 상업용 볶은 커피 원두 (미디엄 로스트 7가지, 다크 로스트 7가지)를 지역 시장에서 구매하여, 선행연구에서 기술된 바와 같이 로스팅된 커피의 화학적 프로파일링을 수행했다 (Gao et al., 2021).
- 콜롬비아산과 코스타리카산 두 종류의 아라비카 커피 생두는 Coffee Bean Corral (미시시피주 매디슨)에서 공급받아, 선정된 화합물들의 생성에 로스팅 프로세스가 미치는 영향을 평가했다.
2.3 Coffee brew sample preparation
- 로스팅된 커피 추출액(roasted coffee brews)은 Gao et al. (2021)에 기술된 바에 따라 마련되었다.
- 간단히 설명하면, 갓 분쇄한 커피 10g을 드립 커피 메이커 (Moccamaster KBT741; Technivorm, Amerongen, 네덜란드)를 사용하여 나노퓨어 워터 200mL로 추출했다.
- 각 커피 샘플을 두 번 추출하여 생물학적 복제물을 준비했다.
- 또한, UPLC/MS nontargeted analysis (非標的 分析)을 위해 각 커피 추출 샘플(n = 14) 10mL를 함께 첨가하여 quality control (QC) 샘플을 제조했다.
- QC 샘플은 샘플 시퀀스에 걸친 기기 성능을 모니터링하는 데 사용된다.
2.4 Coffee green bean roasting preparation
- 콜롬비아산과 코스타리카산 커피 생두를 디지털 드럼 로스터 (Hottop KN-8828B-2K; 미국 코네티컷주 브랜포드)를 사용하여 개별적으로 로스팅했다.
- 구체적으로, 드럼 로스터 내부 온도가 75℃에 도달했을 때 커피 생두 250g을 투입했다.
- 미디엄 로스트의 경우, 10분 로스팅 시간 동안 최대 로스팅 온도가 180 ℃에 도달했다 (Supplement Figure S1).
- 다크 로스트의 경우, 12분 로스팅 시간 동안 최대 로스팅 온도가 210 ℃에 도달했다(Supplement Figure S2).
2.5 Bitter intensity evaluation of coffee brew
- 오하이오 주립대학교 식품과학기술학과에서 8명의 패널리스트(남성 3명, 여성 5명, 연령 23~28세)를 모집했다.
- 커피 브루 평가 전에, 패널리스트들은 카페인 레퍼런스 수용액의 쓴맛 강도를 평가하는 훈련을 받았다.
- 이 훈련은 bitter intensity 2.0(카페인 0.01%), 3.5(카페인 0.02%), 5.0(카페인 0.035%), 6.5(카페인 0.05%), 8.0(카페인 0.065%), 9.5(카페인 0.08%)로 구성된 15점 척도를 사용했다 (World Coffee Research Sensory Lexicon, Version 2.0, 2017).
- 훈련 후 정확성과 일관성을 입증한 패널리스트들이 평가 세션에 참여했다.
- 14가지 커피 브루들의 쓴맛 강도는 Gao et al. (2021)에 기술된 바와 같이 15점 만점의 쓴맛 척도(World Coffee Research Sensory Lexicon, Version 2.0, 2017)를 사용하여 평가했다.
- 요약하자면, 8명의 훈련된 패널리스트(남성 3명, 여성 5명, 연령 23~28세)가 커피 추출액(n = 14)의 쓴맛 강도를 이틀 연속 4회에 걸쳐 두 번씩 평가했다.
- 각 세션에서 7개의 샘플을 평가했다.
- 쓴맛 평가에 후각이 미치는 영향을 방지하기 위해 코 클립을 사용했다.
- 샘플 사이에는 패널리스트들이 무염 크래커와 물을 사용하여 입안을 헹구었고, 샘플 사이에 90초의 휴식을 취했다.
- 데이터는 Compusense Cloud 소프트웨어 (Compusense Inc., Guelph, ON, Canada)를 사용하여 수집했다.
- 센서리 연구 프로토콜은 오하이오 주립대학교 기관윤리위원회(No. 2017H0072)의 승인을 받았다.
2.6 UPLC/MS chemical profiling
- 커피 브루들의 비표적 화학 프로파일링(nontargeted chemical profiling)은
UPLC Waters Acquity H-Class system과
Synapt G2S-IM-QToF mass spectrometer (Waters Co., Milford, MA)를 결합 사용하여 수행되었다. - 샘플 정제 준비, 크로마토그래피 분리 방법 및 질량 분석기 설정은 이전에 Gao et al. (2021)에 기술되어 있다.
- 간략히, 샘플 14가지, 생물학적 복제물 2가지, 기술적 복제품 2가지로 구성된 56개 커피 브루 샘플의 비표적 화학 프로파일을 UPLC/MS-QToF를 사용하여 무작위 순서로 분석했다.
- 또한, 기기 성능을 확인하기 위해 샘플 시퀀스 시작 시와 10개 샘플마다 공시료(blank sample), 컬럼 표준물질, QC 샘플을 일관되게 분석했다.

2.7 Multivariate statistical analysis (MVA)
- UPLC/MS-QToF에서 수집된 크로마토그래피 및 스펙트럼 데이터는
Progenesis QI 소프트웨어 (Nonlinear Dynamics, Durham, NC)를 사용하여
정렬, 디콘볼루션(deconvolution), 이온 추출(ion extraction) 및 적분(integration)을 통해 통계 변수로 변환되었다. - 화학적 특성은
retention time_mass/charge ratio (RT_m/z) 및 이온 강도(and ion intensity) 형식으로 내보내졌다. - QC 샘플에서 이온 강도가 750 미만이고 분산 계수(coefficient of variance)가 20%를 초과하는 특성은
R script version 3.5.2 (R Foundation, Vienna, Austria)를 사용하여 필터링했다. - 그런 다음, 화학적 프로파일링 데이터를
파레토(Pareto) 스케일링한 후,
SIMCA-P+ version 14.1 (Umetrics, Umeå, Sweden)을 사용하여 다변량 데이터 분석을 수행했다. - 구체적으로,
principal component analysis (PCA) 및
orthogonal partial least square (OPLS) regression model을 구축했다. - OPLS 모델에서는 커피 브루의 화학적 프로파일들과 쓴맛 강도 평점들을 각각 x 변수와 y 변수로 사용했다.
- 마지막으로, OPLS의 variable of importance (VIP) 점수와 S-plot을 활용하여
커피 쓴맛 강도에 대한 예측력이 높고 양의 상관관계를 갖는 다섯 가지 화학적 features를 선정했다.
2.8 Off-line Multidimensional preparative-liquid
chromatography/mass spectrometry (Prep-LC/MS) fractionation
- Gao et al. (2021)에서 수정한 Prep-LC/MS를 이용하여
쓴맛 강도가 가장 높은 커피 샘플에서 다섯 가지 화학적 특징(Table 1)을 분리했다. - 추출 방법은 프렌치 프레스 커피 메이커를 사용하여 300g의 분쇄 커피를 3L의 끓는 물에 넣고 15분간 추출하여 선정된 화학적 특징들의 추출 수율을 높이는 방식으로 최적화했다.
- 그 커피 추출액을 원심분리하여 상청액을 수거한 후,
직경 55mm의 qualitative filtration membrane (MilliporeSigma, Burlington, MA)을 통해 추가로 여과했다. - 그런 다음 95% 메탄올/물(v/v) 40mL와 5% 메탄올/물(v/v)로 컨디셔닝한
Oasis HLB 6g bed cartridges (Waters Co., Milford, MA)를 사용하여 샘플을 정제했다. - 여과된 커피 추출액(400mL)을 HLB 카트리지에 넣고 5% 메탄올 100mL를 사용하여 흡착층을 추가로 세척했다.
- 40%, 60%, 80% 메탄올/물(v/v) 60mL를 사용하여 세 가지 분획을 용출했다.
- 마지막으로, Rocket Synergy Purge (Genevac, 영국)를 사용하여
용출액을 용매에서 제거하고 동결 건조했다. - 첫 차원 분획(the first dimension fractionation)의 경우,
동결 건조된 샘플을 10% 메탄올에서 재구성하고, PTFE 0.45µm 필터로 여과한 후,
50mm×50mm Xbridge Prep C18, 5µm particle size column (Waters Co.)을 사용하여,
2525 binary gradient manager (Waters Co.)와
fraction collector 2767 (Waters Co.)이 결합된 Preparative LC/MS-TQD에 주입했다. - 이때 바이너리 이동상은 (A) 0.1% 포름산이 포함된 물과 (B) 0.1% 포름산이 포함된 메탄올이었다.
- Elution gradient는 다음과 같았다 : 0~1분, 10% B 유지; 1~6분, 30%~40% B 유지; 6~26분, 40%~50% B; 26~29분, 50%~95% B; 29~31분, 95% B 유지; 31~31.01분, 95%~10% B; 31.01~33분, 10% B 유지.
- 용출 유속은 100mL/분으로 설정했다.
- 1차 182 dimension separation 과정에서 다섯 가지 화학적 특징들(Table 1)을 개별 분획들로 분리했다.
- First dimension fractions을 모아(pooled) 용매를 제거하고 동결건조한 후,
10% 메탄올에 재구성하고 0.45µm 필터로 여과한 후 추가 분획했다. - 2차 분획의 경우(second dimension fractionation),
각 화학적 features를 분리하기 위해 여러 다른 컬럼들과 용매들을 사용하여 더 높은 순도를 얻었다. - Xselect CSH Prep Phenyl-Hexyl 5 μm OBD 50×100 mm 컬럼 (Waters Co.)을 사용하여,
6.86_537.3426 및 8.44_565.3044 (Table 1)의 화학적 features를 분리했다. - 이 때 (A) 0.1% 포름산을 물에 녹인 용액과 (B) 0.1% 포름산을 메탄올에 녹인 용액의 바이너리 이동상을 100 mL/min의 유속으로 사용했다.
- 6.86_537.3426의 elution gradient는 다음과 같았다: 0~1분, 20%~36% B; 1~22분, 36%~37% B; 22~23분, 37%~95% B; 23~25분, 95% B 유지; 25~25.01분, 95%~20% B; 25.01~27분, 20% B 유지.
- 8.44_565.3044의 elution gradient는 다음과 같았다: 0~1분, 5%~49% B; 1~21분, 49%~53% B; 21~22분, 53%~95% B; 22~24분, 95% B 유지; 24~24.01분, 95%~5% B; 24.01~26분, 5% B 유지.
- 둘째, Xselect CSH Prep Phenyl-Hexyl 5 μm OBD 50×100 mm 컬럼 (Waters Co.)을 사용하여,
화학적 feature 7.38_538.3265 (Table 1)를 분리했다.
이때 (A) 0.1% 포름산 수용액과 (B) 0.1% 포름산 아세톤 수용액의 바이너리 이동상을 100 mL/min의 유속으로 사용했다. - Elution gradient는 다음과 같았다: 0~1분, 10%~22% B; 1~21분, 22%~27% B; 21~22분, 37%~95% B; 22~24분, 95% B 유지; 24~4.01분, 95%~10% B; 24.01~26분, 10% B로 유지.
- 셋째, Atlantis T3 5 μm OBD 50×250 mm 컬럼 (Waters Co.)을 사용하여,
화학적 feature 8.16_598.3258과 8.05_663.4110 (Table 1)을 분리했다. - 이때 바이너리 이동상은 (A) 0.1% 포름산 수용액과 (B) 0.1% 포름산 아세톤 수용액을 100 mL/min의 유속으로 사용했다.
- Elution gradient는 다음과 같았다: 0~1분, 5%~35% B; 1~25분, 35%~40% B; 25~26분, 40%~95% B; 26~28분, 95% B 유지; 28~28.01분, 95%~5% B; 28.01~30분, 5% B로 유지.
- 2차 디멘션 분획(2nd dimension fractions)은
1st dimension fractions에서 사용한 것과 동일한 풀링, 용매 제거, 동결건조, 재구성 및 여과 절차를 사용하여 마련되었다. - 고순도를 달성하기 위해 3차 디멘션 분획법(3rd dimension fractionation)을 적용하여 5가지 화학적 features 각각을 더욱 정제했다.
- Xbridge BEH C18 5 μm OBD 10 mm × 250 mm 컬럼에서 분리를 수행하여, 화학적 features 6.86_537.3426과 8.05_663.4110을 각각 분리했다.
- (A) 0.1% 포름산 수용액과 (B) 0.1% 포름산 메탄올 용액의 바이너리 gradient를 7 mL/min의 유속으로 사용했다.
- 6.86_537.3426을 분리하기 위한 elution gradient는 다음과 같았다: 0~1분, 5%~37% B; 1~26분, 37%~42% B; 26~27분, 42%~95% B; 27~29분, 95% B 유지; 29~29.01분, 95%~5% B; 29.01~31분, 5% B 유지.
- 8.05_663.4110을 분리하기 위한 elution gradient는 다음과 같았다: 0~1분, 10%~47% B; 1~24분, 47%~53% B; 24~25분, 53%~95% B; 25~27분, 95% B 유지; 27~27.01분, 95%~10% B; 27.01~29분, 10% B 유지.
- 둘째, Xselect HSS T3 5 μm OBD 10 × 250 mm 컬럼을 사용하여 7.38_538.3265를 3차 디멘션에서 정제했으며, 이때 (A) 0.1% 포름산 수용액과 (B) 0.1% 포름산 아세톤 수용액의 바이너리 gradient를 7 mL/min의 유속으로 적용했다.
- 그 elution gradient는 다음과 같았다: 0~31분, 26% B 유지; 31~32분, 26%~95% B 유지; 32~34분, 95% B 유지; 34~34.01분, 95%~26% B 유지; 34.01~36분, 26% B 유지.
- 셋째, Xbridge Prep Shield RP18 5 μm 10 × 250 mm 컬럼을 사용하여 (A) 0.1% 포름산 수용액과 (B) 0.1% 포름산 아세톤 수용액의 바이너리 gradient를 7 mL/min의 유속으로 사용하여 8.44_565.3044를 분리했다.
- Elution gradient는 다음과 같았다: 0~27분, 34% B 유지; 27~28분, 34%~95% B 유지; 28~30분, 95% B 유지; 30~30.01분, 95%~34% B 유지; 30.01~32분, 34% B 유지.
- 마지막으로, Xselect CSH Phenyl-Hexyl 5 μm OBD 10 mm × 250 mm 컬럼을 사용하여, (A) 0.1% 포름산 수용액과 (B) 0.1% 포름산 메탄올 수용액의 바이너리 gradient를 7 mL/분의 유속으로 하여 8.16_598.3258을 분리했다.
- Elution gradient는 다음과 같았다: 0~1분, 10%~50% B; 1~22분, 50%~56% B; 22~23분, 56%~95% B; 23~25분, 95% B 유지; 25~25.01분, 95%~10% B; 25.01~27분, 10% B 유지.
- Mass spectrometer의 세팅은 다음과 같았다 : ionization mode = negative, capillary voltage = 2.5 kV, cone voltage = 30 V, cone gas flow rate = 60 L/h, source temperature = 150 ℃, desolvation gas temperature = 350 ℃, 그리고 desolvation gas flow rate = 600 L/h.
- Time based collection을 사용하여 표적 화합물들의 retention time 범위 내에서 1차 디멘션 분획들을 수집했다.
- Single Ion Monitoring (SIR) collection을 사용하여 표적 화합물들의 최적화된 신호 강도를 갖는 2차 및 3차 디멘션 분획들을 수집했다.
2.9 Quantification by
ultra-performance liquid chromatography–tandem mass spectrometry (UPLC–MS/MS)
- 5가지 화합물들의 농도(Table 1)는 Gao et al.(2021)로부터 적용한
UPLC Waters Acquity H-Class system coupled with TQS mass spectrometer (Waters Co.)을
사용하여 커피 샘플에서 측정했다. - 정제된 각 화합물의 알려진 양과 내부 표준물질인 메틸파라벤(methylparaben)을
커피 브루 샘플들에 첨가하여 6-point standard addition curve를 작성했다. - 샘플들 뿐만 아니라 각 보정 레벨에 대해서도 세 가지 생물학적 복제물들이 마련되었다.
- 60% 커피:물 (v/v) 1mL를 HLB 96-well plate에 넣었다.
- 그런 다음, 5% 메탄올:물(v/v) 500μL를 첨가하여 HLB 96-well plate에서 극성 화합물들을 세척했다.
- 마지막으로, 96-well plate로부터 95% 아세토니트릴:물 500μL를 용출하여 분석물들을 UPLC-MS/MS 분석 전에 나노퓨어 워터로 1:10으로 희석했다.
- 콜롬비아산 및 코스타리카산 생두, 미디엄 로스트, 다크 로스트에서도 다섯 가지 화합물을 분석했다.
- 분쇄된 생두 또는 로스트 빈 1g을 15mL 에펜도르프 튜브(Eppendorf tube)에 넣고 50% 메탄올:물(v/v) 10mL와 0.25인치 스테인리스 스틸 믹싱 볼 1개를 넣었다.
- GenoGrinder를 사용하여 1000rpm에서 5분간 혼합했다.
- 그런 다음, 샘플을 10,000rpm에서 10분간 원심분리했다.
- 상청액 100µL를 나노퓨어 워터 900µL로 희석한 후,
위에서 설명한 HLB 96-웰 플레이트를 사용하여 샘플을 정제했다. - 다섯 가지 화합물 모두 Cortecs UPLC C18+ 1.6 μm 2.1 × 100 mm 컬럼에서 (A) 0.1% 포름산(v/v)을 첨가한 물과 (B) 0.1% 포름산(v/v)을 첨가한 아세토니트릴의 바이너리 용매 혼합물을 사용하여 분리했다.
- Gradient는 다음과 같았다: 0~1분, 10%~20% B; 1~8분, 20%~30% B; 8~8.01분, 30%~95% B; 8.01~9.5분, 95% B 유지; 9.5~9.51분, 95%~10% B; 9.51~11분, 10% B 유지. 유속은 0.5 mL/분이었다.
- 질량 분석기 세팅은 다음과 같았다: ESI negative ionization, capillary voltage = 3 KV, cone voltage = 30 V, desolvation temperature = 550 ℃, source temperature = 150 ℃, desolvation gas flow = 1000 L/h, cone gas flow rate = 150 L/h, injection volume = 2 µL.
- 데이터는 Table 1에 나열된 transitions에 따라 Multiple Reaction Monitoring (MRM) 모드를 사용하여 수집했다.
- 18 V collision energy (충돌 에너지), 20 V cone voltage에서 150.95 m/z → 91.85 m/z로의 transition을 사용하여, 메틸파라벤(Methylparaben)이 모든 화합물의 내부 표준물질로 사용되었다.
- 정량화는 6-point standard addition curves를 사용하여 수행했으며, 생물학적 복제물 3개는 모든 화합물들에 있어 R2 > 0.99로 양호한 선형성을 보였다.
2.10 Sensory recombination analysis
- 오하이오 주립대학교 식품과학기술학과에서 10명의 패널리스트(남성 5명, 여성 5명, 연령 24~44세)를 모집했다.
- 샘플 평가 전, 패널리스트들은 Gao et al. (2021)에 기술된 바와 같이, 15점 만점의 쓴맛 평가 척도를 사용하여 카페인 표준 용액의 쓴맛 강도를 평가할 수 있도록 충분한 교육을 받았다.
- 교육 후 정확성과 일관성을 입증한 패널리스트들은 쓴맛 평가 세션에 참여했다.
- 선정된 5가지 예측 화합물들의 혼합물 및 개별 화합물들이 커피 브루의 쓴맛 강도(bitter intensity)에 미치는 영향을 검증하기 위해 3번의 관능 재조합 시험(sensory recombination tests)을 실시했다.
Recombination model 1: 화합물 1~5를 대조군 커피 샘플(쓴맛 강도가 가장 낮음)에 혼합물로 첨가하여 쓴맛이 가장 강한 커피 샘플(표 1)의 농도와 일치시켰다. 다섯 가지 화합물을 함께 첨가해도 커피 샘플의 pH는 변하지 않았다 (pH = 4.95).
Recombination model 2: 화합물 1~5를 대조군 커피 샘플(쓴맛 강도가 가장 낮음)에 개별적으로 첨가하여 쓴맛이 가장 강한 커피 샘플의 농도와 일치시켰다 (Table 1).
Recombination model 3: 화합물 1~5를 0.005 M 인산나트륨 완충액(sodium phosphate buffer solution)(pH 4.95)에 혼합물로 첨가하여 쓴맛이 가장 강한 커피 샘플의 농도와 일치시켰다 (Table 1). - 패널리스트들은 이지택일 (2-alternative forced-choice, 2-AFC) 차이 테스트을 통해 샘플의 쓴맛을 평가한 후,
샘플들의 쓴맛 강도 평점을 매겼다. - 각 재조합 모델과 대조군 샘플 5mL를 뚜껑이 있는 1온스(3자리 숫자로 표시된) 검은색 컵에 나누어 담아
각 패널리스트에게 무작위 제공 순서에 따라 한 쌍으로 제공했다. - 각 쌍에서 패널리스트들은 가장 쓴맛이 강한 샘플을 고른 후,
15-point caffeine bitterness scale (World Coffee Research Sensory Lexicon, 버전 2.0, 2017)를 사용하여
각 샘플의 쓴맛 강도를 평가했다. - 필요한 경우 패널리스트들은 샘플을 다시 맛볼 수 있었다.
- 평가 중에는 후각 반응과의 상호 작용을 방지하기 위해 코 클립을 사용했다.
- 샘플 쌍 사이에는 3분의 휴식 시간을 두었고, 물과 무염 크래커를 미각 세정제로 사용했다.
- 모든 평가는 중복으로 수행되었으며, 데이터는 Compusense Cloud 소프트웨어(Compusense Inc., Guelph, ON, Canada)를 사용하여 수집되었다.
- 센서리 평가 프로토콜은 오하이오 주립대학교 기관윤리위원회(Institutional Review Board)의 승인을 받았다 (2021B0134).
2.11 Consensus sensory analysis of individual compounds
- 패널리스트들에게 각 예측 화합물의 맛 속성을 평가하도록 요청했다.
- 화합물들은 가장 쓴맛이 강한 커피 샘플(Table 1)의 농도로 18.2 MΩ 물에 개별적으로 만들어졌다.
- 패널리스트들에게 각 샘플을 대조군(물)과 비교하여 맛보고 관찰 결과를 기록하도록 지시했다.
- 맛 속성은 패널 합의에 따라 결정되었다.
- 패널리스트들은 커피 분리 후 잔류할 수 있는 잠재적인 후각 상호작용을 방지하기 위해 평가 중 코 클립을 착용했다.
2.12 Nuclear magnetic resonance
- 상용 표준물질이 없었기 때문에, 화합물 1~5 (Table 1)의 화학 구조는
Nuclear Magnetic Resonance (NMR)을 이용하여 분석하였다. - NMR 분석은
Bruker Advance III HD Ascend 분광기에서
z-gradients를 갖는 5 mm triple resonance observe TXO cryoprobe (삼중공명 관측 TXO 저온 탐침)을
사용하여 수행하였다 (1H nucleus의 경우는 700MHz, 13C nucleus의 경우는 176MHz에서 작동)
(Bruker BioSpin, Rheinstetten, Germany). - 각 화합물의 정제된 분말을 용해하기 위해
Deuterated dimethyl sulfoxide-d6 (중수소화 디메틸 설폭사이드-d6)를 용매로 사용하였으며,
화합물 4는 methanol-d4에 용해하였다. - 각 화합물의 NMR 데이터는 보충 자료에 제시되어 있다.
2.13 Data analysis
- SPSS statistics version 25 (IBM, Armonk, NY)가 센서리 데이터 및 정량화 데이터를 분석하는데 사용되었다.
- Student’s t-test (α = 0.05)가 재조합 모델들과 대조군 샘플 간의 쓴맛 강도 평점들을 분석하기 위해 사용되었다.
- One-way ANOVA와 two-way ANOVA (α = 0.05)가 센서리 패널 성과를 평가하기 위해 수행되었다.
3. Results and Discussion
3.1 Multivariate statistical modeling
- 데이터 처리 후 커피 브루 샘플들로부터 1,680개의 chemical features가 수집되었다.
- Goodness of fit (R²X = 0.99)과 predictive power (Q² = 0.97)을 갖는
非指導 PCA 모델(unsupervised PCA model)을 먼저 생성하여,
샘플들의 클러스터들을 시각화하고 샘플 이상치(outliers)를 파악했다 (Supplement Figure S3). - 일반적으로, 서로 다른 샘플들이 분리되어, 샘플 간의 화학적 차이가 포착되었음을 나타냈다.
- 다음으로, 높은 적합도(R²Y = 0.95)와 예측력(Q² = 0.91)을 갖은
bitter intensity scores (Y 변수)와 상관관계가 있는 화학적 프로파일링 데이터(X 변수)의 변차(variations)를
구분하기 위해 supervised orthogonal partial least squares (OPLS) 모델을 구축했다. - 일반적으로 Q² > 0.5인 PLS 모델은 비표적 대사체학 연구에서 허용 가능한 예측력으로 간주된다
(Eriksson et al., 2013; Wold et al., 2001). - Figure 1은
OPLS 모델의 예측 플롯(predictive plot)을 보여주며,
15점 중 0.28의 root mean squared error of prediction (RMSEP) (예측오차의 평균제곱근)로
기존 OPLS 모델의 높은 정확도를 보여준다. - 또한, permutation test (R² = 0.41, Q² = -0.55) 결과, OPLS 모델의 과적합(overfitting)은 나타나지 않았다.

- Bitter intensity에 대해 높은 예측성을 보이며 양의 상관관계를 나타낸 화학적 features (RT_m/z)가
predictive variable of importance (VIP) 값을 기반으로 선정되었다. - VIP 값은 X 변수(화학적 특성)가 Y 변수(쓴맛 강도 점수) 예측에 미치는 영향을 설명한다.
- 일반적으로 VIP 값이 1보다 큰 X 변수는 유의미한 기여를 하는 것으로 간주된다 (Galindo‐Prieto et al., 2014).
- Figure 2에는 S-plot이 제시되어 있으며, 샘플들 간 각 X 변수의 변화 크기와 그리고 각 X 변수와 Y 변수의 상관관계를 시각화한다.
- 최종적으로 VIP 값이 4 이상(Table 1)이고, 커피 브루에서 쓴맛 강도와 높은 공분산 및 상관관계를 보이는 5가지 화학적 특성들(6.86_537.3426, 7.38_538.3265, 8.05_663.4110, 8.16_598.3258, 8.44_565.3044)을 추가 분석을 위해 선정한 후, 각각 화합물 1~5로 표시했다.

3.2 Isolation and identification of positively correlated compounds
- 처음의 MS 스펙트럼 분석 및 라이브러리 검색 결과, 화합물 1~5는 신규 생성물인 것으로 나타났다.
- 그 화합물들은 먼저 커피 브루로부터 추출한 후, 오프라인 다차원 분취용 LC/MS 시스템(off-line multi-dimensional preparative LC/MS system)을 사용하여 개별적으로 분리했다.
- 각 화합물의 순도는 UPLC/MS-QToF를 사용하여 음성 및 양성 ESI 모드에서 total ion chromatogram peak area로 모니터링했으며, 1H NMR 분석을 통해 화합물 1, 2, 3, 4, 5의 순도가 각각 92%, 98%, 93%, 90%, 87%임을 확인했다.
- 그 화합물들의 구조 해석은 UPLC/MS-QToF 및 1D 및 2D NMR 분석을 통해 수행했다.
- MS 및 NMR 스펙트럼 분석을 바탕으로, 화합물 1~5의 구조(Table 1)를 성공적으로 규명하여 Figure 3에 나타냈다.

3.2 Isolation and identification of positively correlated compounds
- 화합물 1은 C26H46N6O6의 원소 조성(∆m/z = 3.6 ppm)을 갖는 m/z 537.3426 [M-H]–를 보고했으며, ESI+ 모드에서 MS/MS 이온 조각은 522 m/z, 494 m/z, 409 m/z, 381 m/z, 296 m/z로 Figure 3a에 제시된 분자와 일치했다.
- 이 조각들 중 494 m/z [M-44]+는 말단 아미드基(a terminal amide group)의 손실에 해당한다.
- 1H 및 371 13C NMR 분석 결과,
펩타이드 결합의 아미드基들에 속하는 6개의 4차 탄소(δ 177.4, 173.9, 172.2, 172.0, 171.8, 171.4 ppm)인
7개의 CH3, 5개의 CH2, 8개의 CH3, 그리고 6개의 qC가 존재함을 보여주었다 (Supplement Figure S4). - 또한, 7개의 메틸基(methyl groups) 중
4개(δ 0.87(m, 6H)/δ 22.9(C-14), 23.0 ppm(C-26); δ 0.82(m, 6H)/δ 21.5(C-13), 21.6 ppm(C-25))는
1H-1H COSY correlations에서 확인된 바와 같이
두 개의 L-Leucine 아미노산에 존재하는 두 개의 이소프로필基(isopropyl groups)에 해당한다. - 마찬가지로, δ 1.20(dd, J = 7.1, 2.4 Hz, 3H)/δ 17.9 ppm(C-20); δ 0.82(m, 3H)/δ 21.7 ppm(C-19)에서 공명하는
두 개의 메틸基는 한 L-Isoleucine 아미노산의 sec-butyl group에 속하고, δ 0.87(m, 3H)/δ 23.01 ppm(C-8)의 마지막 메틸基는 L- L-Alanine 아미노산에 해당한다. - 또한, 하나의 주요 스핀 시스템(key spin system)은 δ 4.05(td, J = 8.4, 4.3 Hz, 1H)/δ 55.3 ppm(C-4)에서 공명하는 하나의 메틴基(methine group)와, δ 2.22(ddt, J = 12.6, 10.2, 8.4 Hz, 1H), δ 1.88(m, 1H)/δ 25.1 ppm(C-3)에서 공명하는 하나의 부분입체이성질성 메틸렌基(diastereotopic methylene group), 그리고 δ 2.16 – 2.02(m, 2H)/δ 29.2 ppm(C-2)에 위치한 또 다른 메틸렌基 간의 1H-1H COSY correlations를 사용하여 결정되었다.
- 또한, HMBC 실험은 δ 177.4 ppm (C-1)에 위치한 L-Glutamic 아미노산의 카르복실基(carboxyl group)의 4기로 된 탄소(quaternary carbon)를 가진 두 메틸렌基들 사이의 중요한 교차 피크 상관관계(key cross peak correlation)를 보여, L-Glutamic acid의 정체를 확인했다.
- δ 4.05 (td, J = 8.4, 4.3 Hz, 1H)/δ 55.3 ppm(C-4)에서 공명하는 L-Glutamic acid 내의 α-methine과, δ 177.4 ppm(C-1)에 위치한 L-Glutamic acid의 quaternary carbon 사이의 핵심적인 HMBC cross peak correlation (교차 피크 상관관계)를 통해, 고리형 ɣ-락탐(cyclic ɣ-lactam)의 형성을 확인할 수 있다 (Supplement Figure S9).
- 마지막으로, 다양한 아미노산들(L-Glu, L-Ala, L-Leu, L-Ile, L-Leu)의 모든 α-메틴 신호(α-methine signals)는 Figure 3에서 볼 수 있듯이, quaternary carbons (amide groups)와 특정 핵심 상관관계를 보였다.
- 모든 단차원 및 2차원 NMR 분석을 바탕으로, 화합물 1의 구조는 Figure 3a와 같이 규명되었으며,
((S)-5-oxopyrrolidine-2-carbonyl)-L-alanyl-L-leucyl-L-isoleucyl-L-leucyl-(S)-2-amino-4-methylpentanamide로 명명되었다. - 우리가 아는 한, 커피에서 분리된 이 펩타이드는 새로운 화합물이다.
- 화합물 2의 m/z는 538.3265 [M-H]–였으며, 원소 조성은 C26H45N5O7 (∆ m/z = 4.2 ppm)이었다.
- ESI+ 모드에서 MS/MS 이온 조각들(ion fragments)은 522 m/z, 494 m/z, 409 m/z, 381 m/z, 296 m/z로 화합물 1에서 나타난 것과 유사했으며, 이는 화합물 1과 화합물 2 사이의 구조적 유사성을 시사한다 (Figure 3a-b).
- 1H 및 13C NMR 분석 결과도 화합물 1과 화합물 2 사이의 유사성을 보여주었다 (Supplement Figure S5).
- 예를 들어,
7 CH3, 5 CH2, 8 CH 및 6 qC,
펩타이드 결합의 아미드基들에 해당하는 6개의 quaternary carbons (δ 177.9, 175.0, 172.5, 172.2, 172.1, 170.7 ppm),
2개의 이소프로필基 (isopropyl groups) (δ 0.87(t, J = 7.2 Hz, 6H)/δ 23.7(C-14) 및 23.6 ppm(C-26), 0.83(m, 6H)/δ 23.5(C-13) 및 22.9 ppm(C-25))의 존재 (→ L-Leucine 아미노산의 존재를 가리킴),
sec-butyl chain 내의 δ 1.20(d, J = 7.1 Hz, 3H)/δ 1.20 ppm(C-20)과 δ 0.83(m, 3H)/δ 22.2 ppm(C-19)에 위치한 메틸基 (→ 2개의 L-Leucine 아미노산 존재를 가리킴),
그리고 δ 0.81(d, J = 6.5 Hz, 3H)/δ 22.1 ppm(C-8)에 위치한 메틸 1개는 1H- 1H COSY correlations에 의해 입증된 바와 같이 L-Alanine 아미노산에 해당한다. - 또한, δ 4.05(td, J = 8.7, 4.0 Hz, 1H)/δ 55.8 ppm(C-4)에 위치한 메틴基에서
L-Glutamic acid의 동일한 주요 스핀 시스템(spin system )이 결정되었으며,
이는 δ 2.25 – 2.17(m, 1H), δ 1.88(ddt, J = 13.5, 9.3, 4.6 Hz, 1H)/δ 25.6 ppm(C-3)에서 공명하는 하나의 부분입체이성질성 메틸렌基(one diastereotopic methylene group)와, 그리고
마지막으로 δ 2.08(m, 1H), 2.05(ddd, J = 16.0, 9.9, 5.2 Hz, 1H)/δ 29.6 ppm(C-2)에서 공명하는 메틸렌基와 상관관계가 있었다. - 마찬가지로, 화합물 1의 경우,
L-Glutamic acid의 δ 4.05(td, J = 8.7, 4.0 Hz, 1H)/δ 55.8 ppm(C-4)에 위치한 α-메틴과,
L-Glutamic acid의 δ 177.9 ppm(C-1)에 위치한 4차 탄소 사이의 주요 HMBC 상관관계를 통해,
고리형 ɣ-락탐(cyclic ɣ-lactam)의 형성을 확인할 수 있다 (Supplement Figure S9). - 화합물 1과 화합물 2의 주요 차이점은
화합물 1의 δ 173.9 ppm(C-22)에 위치한 말단 아미드 대신, 화합물 2의 δ 175.0 ppm(C-22)에 위치한 말단 카르복실산基(carboxyl acid group)가 존재한다는 점이며, 이는 MS/MS 분석에서도 말단 카르복실산의 손실에 해당하는 494 m/z [M-45]+ 단편을 통해 확인되었다. - 마지막으로,
여러 다른 아미노산들(L-Glu, L-Ala, L-Leu, L-Ile, L-Leu)의 모든 α-메틴 신호(methine signals)는
Supplement Figure S9에서 볼 수 있듯이 quaternary carbons(아미드基)와 특정 핵심 상관관계를 보였다. - 모든 단차원 및 2차원 NMR 분석을 통해 Figure 3b에 나타난 바와 같이 화합물 2의 구조를 규명할 수 있었다.
- 우리가 아는 한, 커피에서 분리한 이 펩타이드는 새로운 화합물이며,
((S)-5-oxopyrrolidine-2-carbonyl)-L-alanyl-L-leucyl-L-isoleucyl-L-leucine으로 식별되었다. - 화합물 3은
C30H52N10O7(∆ m/z = 1.52 ppm)의 원소 조성을 갖는 m/z 663.4110 [M-H]–를 보고했다. - ESI+ 모드 550 m/z, 522 m/z, m/z 및 423 m/z의 MS/MS ion fragments는 Figure 3c에 나타난 펩타이드 구조와 일치했다.
- 1H 및 13C NMR 분석 결과,
펩타이드 결합의 8개 4차 탄소(δ 177.4, 172.3, 171.6, 171.5, 170.9, 170.6, 170.5 ppm) 아미드基들 중
7개에 해당하는 5개의 CH3, 9개의 CH2, 8개의 CH3, 그리고 8개의 qC( Supplement Figure S6)가 존재하는 것으로 나타났다. - 그리고 δ 168.6 ppm(C-25)에 위치한 나머지 quaternary carbon은 이민基(imine group)에 해당하며,
이는 L-Arginine 아미노산의 존재를 나타낸다. - 또한, 5개의 메틸基 중에서, 4개 δ 0.87(d, J = 6.6 Hz, 3H)/δ 23.0 ppm(C-13); 0.84(m, 6H)/δ 21.7(C-12), 18.4ppm(C-19); 0.77(m, 3H)/δ 15.3ppm(C-18)는
2개의 L-Leucine 아미노산들의 두 이소프로필基(isopropyl groups)에 해당하고,
δ 0.93(d, J = 6.7Hz, 3H)/δ 19.2ppm(C-7)에 위치한 최종 메틸基는
1H-1H COSY correlations에 의해 결정된 바와 같이 L-Alanine 아미노산에 할당되었다. - 또한, δ 4.32(q, J = 7.8 Hz, 1H)/δ 56.8 ppm(C-23)에서 공명하는 하나의 메틴基와
δ 2.39(m, 1H), δ 2.21(ddt, J = 12.6, 9.9, 8.6 Hz, 1H)/δ 40.8 ppm(C-22), 1.99 – 1.91(m, 1H), 1.89 – 1.82(m, 1H)/δ 30.2 ppm(C-21), δ 3.63(m, 1H), 3.51(m, 1H)/δ 46.5 ppm(C-20)에 위치한 세 개의 연속적인 메틸렌基 간의 1H-1H COSY correlations를 사용하여 하나의 주요 스핀 시스템(key spin system)이 확립되었으며, 이는 L-Proline 아미노산의 존재를 나타낸다. - 또한, L-Proline 아미노산의 α- α-methine (C-23)과, δ 168.6 ppm에 위치한 L-Arginine 아미노산 내의 이민基(imine group) quaternary carbon (C-25) 사이의 주요 HMBC 상관관계를 통해, 이 두 아미노산과 형성된 고리(the cyclic) 사이의 연결성을 확인할 수 있다 (Figure 3c).
- 마지막으로, 여러 다른 아미노산들(L-Arg, L-Asn, L-Ala, L-Leu, L-Leu, L-Pro)의 모든 α 시그날들은
그들의 qC (carboxyl groups)와 특정 주요 상관관계를 보였다 (Supplement Figure S9 참조). - 모든 단일 및 이차원 NMR 분석을 바탕으로, Figure 3c에 나타난 바와 같이,
화합물 3의 구조가 규명되었으며, 커피에서 분리한 이 펩타이드는 새로운 화합물이며,
Cyclo(L-Arginyl-L-Prolyl-L-leucyl-L-leucyl-L-Alanyl-L-Asparagyl) derivative로 명명되었다. - 화합물 4의 m/z는 598.3258 [M-H]–이고, 원소 조성은 C31H45N5O7 (∆m/z = 2.9 ppm)이었다.
- ESI+ 모드에서 MS/MS ion fragments 554 m/z, 485 m/z, 359 m/z, 240 m/z 또한 Figure 3d에 나타난 펩타이드 구조와 일치했다.
- 마찬가지로, 1H 및 13C NMR 분석 결과, 4개의 CH3, 8개의 CH2, 12개의 CH3, 그리고 7개의 qC가 존재함을 보여주었는데 (Supplement Figure S7), 이는 펩타이드 결합의 7개 quaternary carbons 중 5개 (δ 181.6, 174.7, 174.1, 172.8, 171.9, ppm) amide groups이며, 이는 화합물 4의 펩타이드 성질(peptidic nature)을 가리킨다.
- δ 179.4 ppm(C-1)과 138.3 ppm(C-9)에 위치한 나머지 두 개의 quaternary carbons는 각각
카르복실산基(carboxylic acid group)와 quaternary aromatic carbon에 배정된다. - 추가적으로,
δ 0.96~0.95(m, 6H)(C-20, C-26)와 δ 0.95~0.93(m, 6H)(C-19, C-25)에서 공명하는 4개의 메틸기를 확인하여
두 개의 L-Leucine 아미노산에 할당했다. - 또한, 1H-1H COSY correlations를 사용하여 두 가지 주요 스핀 시스템을 결정했는데,
그 중 하나는 δ 7.24(m, 4H)/δ 130.5 ppm(C-10, C-14), 129.3 ppm(C-11, C-13), 그리고 7.18(m, 1H)/δ 127.7 ppm(C-12)에서 공명하는 5개의 방향족 메틴基(aromatic methine groups)에 의해 형성되어 L-Phenylalanine 아미노산의 존재를 나타내고,
두 번째는 δ 4.33(dd, J = 8.5, 4.0 Hz, 1H)/δ 63.1 ppm(C-2)에서 공명하는 하나의 메틴基와 δ 2.17 – 2.08(m, 2H)/δ 30.5 ppm(C-3), δ 1.98(m, 1H), 1.89(s, 1H)/δ 25.9 ppm(C-4), 및 δ 3.64(m 2H)/δ 48.2 ppm(C-5)에 위치한 3개의 메틸렌基(methylene groups)에 의해 형성되어 L-Proline 아미노산의 존재를 나타낸다. - 또한, 1H-1H COSY 및 HMBC 실험은,
δ 4.16(td, J = 8.9, 4.4 Hz, 1H)/δ 57.9 ppm(C-28)에 위치한 메틴기와
δ 2.43 – 2.32(m, 2H)/δ 30.8 ppm(C-29), δ 2.27(m, 1H), δ 1.99(m, 1H)/δ 30.5 ppm(C-30)에서 공명하는 2개의 메틸렌基 사이에 주요 교차 피크 상관관계가 있음을 보여주었다. - 추가적으로, δ 4.16(td, J = 8.9, 4.4 Hz, 1H)(C-28)과 δ 179.4 ppm(C-27)에 위치한 quaternary carbon 사이의 주요 HMBC 상관관계는 L-Glutamic acid 아미노산을 확인시켜 주었다.
- 그리고, δ 4.66(m, 1H)/δ 55.5 ppm(C-16)에서 공명하는 L-Leucine 아미노산의 α-메틴과, δ 174.1 ppm(C-31)에 위치한 L-Glutamic acid의 quaternary carbon 사이의 주요 HMBC 상관관계를 통해, 이 두 아미노산과 그 형성된 고리 사이의 연결성을 확인할 수 있었다 (Supplement Figure S9).
- 마지막으로, 여러 다른 아미노산(L-Pro, L-Phe, L-Leu, L-Leu, L-Glu)의 모든 α-메틴 신호는 아미드基들의 quaternary carbons와 특정 상관관계를 보였으며, 이는 Supplement Figure S9에 제시되어 있다.
- 모든 단일 및 이차원 NMR 분석을 바탕으로, 화합물 4의 구조가 밝혀졌고,
Figure 3d에 나타난 바와 같이
(6-amino-3-isobutyl-2,5,9-trioxo-1,4-diazonan-1-yl)-4-methylpentanoyl)-L-phenylalanyl-L-proline으로
명명되었으며, 이는 커피에서 분리된 새로운 화합물이다. - 마지막으로, 화합물 5의 경우,
MS 정밀 질량 분석 결과, m/z 값이 565.3044 [M-H]–였으며,
원소 조성은 C30H46O10(∆ m/z = 1.01 ppm)이었다. - MS/MS fragmentation (negative ESI mode) 결과,
301.18 m/z와 481.24 m/z의 단편 이온들(fragment ions)이 관찰되었으며,
이는 2-O-β-D-glucopyranosyl-atractyligenin (2-GA) 분자의 단편화 패턴과 일치했다 (Gao et al., 2021). - 주요 1H NMR(700 MHz, DMSO) 신호는
엑소메틸렌(exomethylene) δ 5.06(s, 1H), δ 4.96(s, 1H)의 존재를 나타냈다 (Supplement Figure S8). - 5개의 카르비놀 메틴(carbinolic methines)이
δ 4.35(dd, J = 11.7, 2.0 Hz, 1H), δ 4.21(dd, J = 7.8, 3.4 Hz, 1H), δ 4.02(tq, J = 11.2, 6.7, 4.5 Hz, 1H), δ 3.94(td, J = 11.3, 7.6 Hz, 1H), δ 3.62(s, 1H)에서 공명하는 것으로 확인되었으며, 이는 당 부분(sugar moiety)과 일치한다. - δ 4.21(d, J = 7.8 Hz, 1H)에 위치한 신호는 아노머 양성자(anomeric proton)에 해당하며, δ 3.62(s, 1H)에 위치한 신호는 디테르펜 골격 구조의 히드록시基에 해당한다.
- δ 0.88(d, J = 6.6 Hz, 6H)에서의 두 피크는 그들의 다중성(multiplicity)과 결합 상수(coupling constants)를 기반으로 볼 때, 당 사슬(sugar chain)에 위치한 이소프로필基(isopropyl group)와 일치했다.
- 당 메틴기(sugar methine group)와 카르복실基의 quaternary carbon 사이의 주요 HMBC 상관관계를 통해, Figure 3e에 나타난 것처럼 두 부분 사이의 연결성을 확인할 수 있다.
- 화합물 5의 모든 신호는 이전에 보고된 화합물
Atractyloside III (Richter & Spiteller, 1978)의 NMR 데이터와 일치했다. - NMR 분석과 MS 단편화 모두 화합물 5가 Gao et al.(2021)에서 이전에 보고된
쓴맛 차단제(bitter blocker) 2-GA의 부가생성물(adduct)임을 보여주었다.
3.3 Quantification of positively correlated compounds
- 화합물 1~5의 농도는 강도 점수가 각각 5.0과 9.4인 저-쓴맛 커피와 고-쓴맛 커피에서 측정되었으며, Table 1에 제시되어 있다.
- 일반적으로, 각 화합물의 농도는 OPLS 모델에서 커피 쓴맛 강도와 陽의 상관관계가 보고된 것을 바탕으로, 예상한 대로 저-쓴맛 커피보다 고-쓴맛 커피에서 유의미하게 높았다.
- 예를 들어, 화합물 2의 함량은 저-쓴맛 커피와 고-쓴맛 커피에서 각각 0.37mg/L와 2.94mg/L로, 두 샘플 간의 농도 차이가 8배에 달했다.
- 마찬가지로, 화합물 1, 3, 4의 경우 저-쓴맛 커피와 고-쓴맛 커피 샘플 간에 농도 변화가 10배 이상 관찰되었다.
- 마지막으로, 화합물 5는 저-쓴맛 커피와 고-쓴맛 커피 샘플 간에 농도 변화가 2배 미만인 유일한 화합물이었다.
3.4 Sensory recombination analysis of positively correlated compounds
- 일련의 sensory recombination tests를 통해 화합물 1~5가 커피 쓴맛에 미치는 센서리 관련성을 조사했다.
- 먼저, 대조군 커피에 화합물 1~5를 혼합물로 첨가했을 때의 영향을 평가했다.
- Recombination model 1은
고-쓴맛 커피에서 정량화된 농도(Table 1)로 대조군 샘플(저-쓴맛 커피 샘플)에 화합물 1~5를 첨가하여 준비했다. - 차이 검정 결과, 그 혼합물 재조합 모델은 대조군보다 유의하게 더 쓴맛이 강했으며 (p = 0.01), 20회 중 16회에서 대조군보다 더 쓴맛이 강한 것으로 나타났다 (2-AFC).
- 또한, 혼합물 재조합 모델의 쓴맛 강도는 6.2로 평가되었는데, 이는 대조군 샘플의 쓴맛 강도인 5.3보다 유의하게 높았다 (p < 0.01, Figure 4).
- 따라서 화합물 1~5를 첨가하면 쓴맛 강도가 0.9 포인트 증가하여 커피 쓴맛에 미묘하지만 관찰 가능한 유의미한 변화가 나타났다.
- 이후, 각 화합물 1~5가 커피의 쓴맛에 미치는 영향을 평가했다.
- 화합물 1~5를 고-쓴맛 커피에 각각의 농도로 (Table 1) 커피 대조군(저-쓴맛) 시료에 개별적으로 첨가하여
5가지 재조합 모델(2a~e)을 만들었다. - 모든 재조합 모델에서 방향 차이 검정(directional difference test)이나 쓴맛 강도 평점들에서 쓴맛 지각에 유의미한 차이가 보고되지 않았다 (p > 0.05).
- 이러한 차이의 부재는 개별 화합물 1~5가 커피의 쓴맛 강도에 영향을 미치지 않았음을 나타낸다.
- 결과적으로, 화합물 1~5는 커피에 혼합하여 제공되었을 때만 쓴맛 지각을 유의미하게 향상시키는 것으로 보고되었으며, 개별적으로 제공되었을 때는 그렇지 않았다.
- 또한, 5명의 숙련된 커피 센서리 패널리스트들이 고-쓴맛 커피 시료에 정량화된 농도로(Table 1) 물에 담긴 각 화합물의 맛 특성을 개별적으로 평가했다.
- 물에 함유된 화합물 1~5에 대한 맛 속성들은 보고되지 않았다.
- 화합물 1-5가 커피 혼합물로 사용되었을 때 관찰된 쓴맛 증진(bitterness enhancement)의 기전을 더욱 자세히 평가하기 위해, 커피 샘플의 pH(4.9)로 완충된 aqueous recombination model을 사용하여 화합물 1-5 혼합물이 지각 가능한 쓴맛을 가지는지 여부를 조사하는 추가 센서리 검사를 수행했다.
- 방향 차이 검정이나 쓴맛 강도 평점들에서 모델 샘플과 대조군(완충수) 샘플 간의 쓴맛 강도에 유의미한 차이가 발견되지 않았다 (p > 0.05).
- 이는 화합물 1-5 혼합물이 지각 가능한 쓴맛을 부여하지 않음을 보여준다.
- 따라서 화합물 1-5는
커피의 쓴맛 지각을 증진시키는 것으로 보고되었는데,
이는 아마도 수용체 조절(receptor modulation)을 통해
커피 내 쓴맛 수용체 작용제(bitter receptor agonists)의
결합 친화도(binding affinity) 및/또는 효능(efficacy)이 증가했기 때문일 것이다 (Schwartz & Holst, 2007). - 모든 재조합 모델에 대한 감각 데이터를 검토한 결과,
패널 재현성과 개념 정렬(concept alignment)이 양호했으며,
샘플의 반복 효과, 샘플 간 상호 작용, 샘플과 패널리스트 간 상호 작용은 p > 0.05로 유의하지 않았다. - 이는 모든 패널리스트가 샘플 간의 쓴맛 지각에 대해 일치했으며,
복제물들 간의 쓴맛 강도를 일관되게 평가할 수 있음을 나타낸다. - 식별된 화합물 5인 아트락틸로사이드(Atractyloside) III의 화학 구조를 추가로 검토한 결과,
2-O-β-D-glucopyranosyl-atractyligenin (2-GA) 부분이 확인되었다 (Figure 3). - 흥미롭게도, Gao et al. (2021)은 커피의 쓴맛을 억제하는 세 가지 화합물 중 하나로 2-GA를 보고했다.
- 아트락틸로사이드(Atractyloside) III의 발생이
지각된 쓴맛 강도와 높은 예측성을 보이며 양의 상관관계를 보이는 것은
Atractyloside III가 2-GA로 분해되거나, 반대로
2-GA에서 Atractyloside III가 생성되는 것과 관련된 간접적인 상관관계로 설명될 수 있다. - 아트락틸로사이드(Atractyloside) III가
커피의 쓴맛 강도에 직간접적으로 영향을 미치는지 여부를 밝히기 위해서는 추가 연구가 필요하다. - 인간의 쓴맛 인지에 관여하는 것으로 알려진 TAS2R 수용체는 약 25종이다
(Behrens & Meyerhof, 2006; Chandrashekar et al., 2000; Meyerhof, 2005). - 그러나 TAS2R 수용체들은
조절 폭(tuning breadth)과 선택성(selectivity) 측면에서 다양한 차이를 보인다 (Meyerhof et al., 2010). - Brockhoff와 동료들은
천연 화합물이 쓴맛 수용체의 작용제와 길항제로 동시에 작용할 수 있음을 발견했다 (Brockhoff et al., 2011). - 예를 들어, 3β-hydroxydihydrocostunolide (3β-하이드록시디하이드로코스투놀리드)는
다양한 TAS2R 수용체들을 자극할 수 있지만,
구조적으로 관련되거나 관련되지 않은 화합물을 포함한 다른 쓴맛 자극에 의한 TAS246의 활성화를 억제하는 것으로 나타났다. - 이와 같이, 쓴맛 지각(bitter perception)은
식역치 이상의 화합물에 대한 가산적 메커니즘(additive mechanisms) 이상의 영향을 받는다. - 본 연구에서 화합물 1~5는 혼합물로서 쓴맛 지각에 상당한 변화를 보고했지만 개별적으로는 그렇지 않았다.
- 이는 커피에서 화학적 자극과 쓴맛 지각 간의 복잡한 상호작용을 뒷받침한다.
- 더욱이, 가장 예측 가능한 陽의 상관관계를 가진 화합물 1~5를 검토한 결과,
커피의 쓴맛 화합물로 이전에 보고된 바는 없었다. - 분석된 샘플에서 알려진 쓴맛 화합물이 커피의 쓴맛과 양의 상관관계(선형 관계)를 보이지 않았다는 관찰 결과는 완전히 예상치 못한 것은 아니다.
- 일반적으로 커피의 쓴맛은 로스팅 수준이 높아질수록 증가하는 것으로 알려져 있다 (Farah, 2019).
- 그러나 로스팅 중 생성되는 카페욜퀴나이드(caffeoylquinides)와 같은 쓴맛 화합물들은 시간이 길어지고 온도가 높아질수록 더욱 분해되어(Blumberg et al., 2010), 비선형 관계를 나타낸다.
- 본 연구에서 사용된 커피 빈들은 원산지들이 다르며 다양한 조건들에서 로스팅 되었다.
- 커피의 잘 알려진 쓴맛 화합물인 카페인 (Chen, 1979)은
선행 연구에서 14가지 커피 샘플들과 해당 쓴맛 강도들 사이에 유의미한 상관관계가
없는 것으로 보고되었다 (Gao et al., 2021). - 또한, 최근 아라비카 커피 생두에서 발견된 강력한 쓴맛 성분인 모잠바이오사이드가
로스팅 과정에서 분해되는 것으로 보고되었다 (Lang et al., 2015).
3.5 Impact of roasting on the generation of compounds 1–5
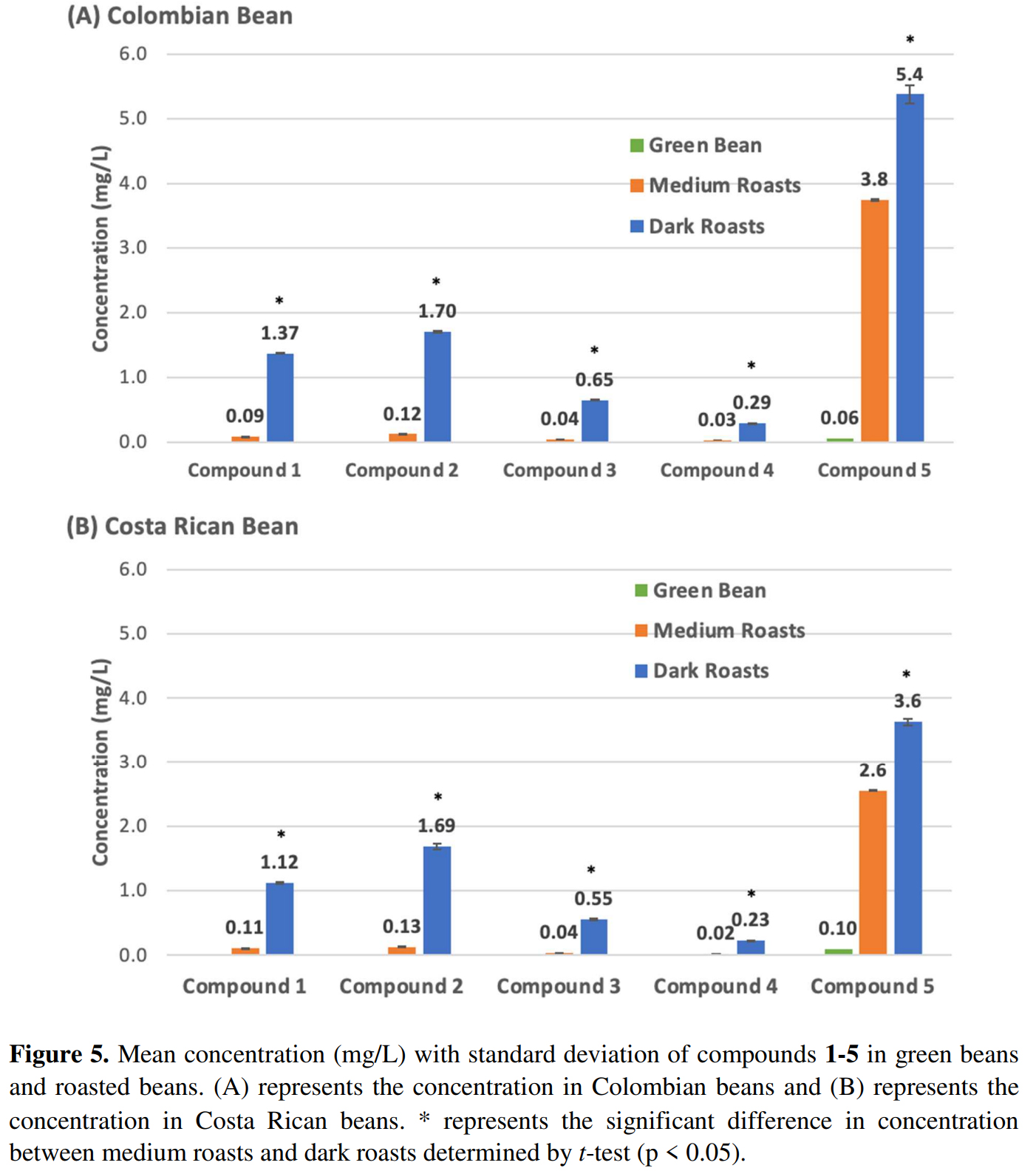
- 화합물 1~5rk 생두(비로스팅), 중배전, 그리고 강배전 원두에서 정량화되어 Figure 5에 제시되어 있다.
- 콜롬비아와 코스타리카産 아라비카 커피 두 품종을 선정했다.
- 5가지 화합물 중 1가지인 화합물 5만 생두에서 검출되었다.
- 따라서 화합물 1~4는 주로 원두 로스팅 과정에서 생성되었다.
- 화합물 1~4의 농도 수준을 검토한 결과,
중배전에서 강배전으로 갈수록 화합물 1~4의 농도가 10배 이상 증가하는 것으로 나타났으며,
화합물 5는 생두에 비해 중배전에서 25배 이상 증가하는 것으로 나타났다. - 쓴맛을 증가시키는 화합물 1~5의 열에 의한 생성(thermal generation)은
더 높은 로스팅 레벨들에서 커피의 쓴맛이 증가하는 것으로 알려진 사실과 일치했다.
4. Conclusion
커피의 쓴맛에 기여하는 새로운 화합물을 비표적 LC/MS 프로파일링 접근법을 사용하여 향미를 발견하여 동정했다.
이 다섯 가지 화합물은 수용액에서는 지각 가능한 쓴맛을 유발하지 않는 것으로 보고되었지만, 커피에 첨가했을 때 수용체 조절 활성에 의해 쓴맛 강도가 증가한 것으로 추정된다.
이러한 결과는 화학적 자극과 쓴맛 지각 사이의 복잡한 상호작용을 더욱 뒷받침한다.
또한, 쓴맛을 증가시키는 그 화합물들은 주로 커피 로스팅 과정에서 생성되는 열 반응 산물인 것으로 보고되었다.
References
Behrens, M., & Meyerhof, W. (2006).
Bitter taste receptors and human bitter taste perception.
Cellular and molecular life sciences: CMLS, 63(13), 1501-1509.
Belitz, H. (1977).
Taste-active substances in coffee. International Coffee Science Association, 7th Colloquium,
Blank, I., Sen, A., & Grosch, W. (1991).
Aroma impact compounds of Arabica and Robusta coffee. Qualitative and quantitative investigations.
14th International Scientific Colloquium on Coffee,
Blumberg, S., Frank, O., & Hofmann, T. (2010).
Quantitative studies on the influence of the bean roasting parameters and hot water percolation on the concentrations of bitter compounds in coffee brew.
Journal of Agricultural and Food Chemistry, 58(6), 3720-3728.
Breslin, P., & Beauchamp, G. (1995).
Suppression of bitterness by sodium: variation among bitter taste stimuli.
Chemical senses, 20(6), 609-623.
Brockhoff, A., Behrens, M., Roudnitzky, N., Appendino, G., Avonto, C., & Meyerhof, W. (2011).
Receptor agonism and antagonism of dietary bitter compounds.
Journal of Neuroscience, 31(41), 14775-14782.
Calvino, A. M., García-Medina, M. R., & Cometto-Muniz, J. E. (1990).
Interactions in caffeine–sucrose and coffee–sucrose mixtures: evidence of taste and flavor suppression.
Chemical senses, 15(5), 505-519.
Chandrashekar, J., Mueller, K. L., Hoon, M. A., Adler, E., Feng, L., Guo, W., Zuker, C. S., & Ryba, N. J. (2000).
T2Rs function as bitter taste receptors.
Cell, 100(6), 703-711.
Charve, J., Chen, C., Hegeman, A. D., & Reineccius, G. A. (2011).
Evaluation of instrumental methods for the untargeted analysis of chemical stimuli of orange juice flavour.
Flavour and fragrance journal, 26(6), 429-440.
Chen, W. (1979).
Studies on the bitter taste of roasted coffee. Relationship between structure and bitter taste of some organic compounds.
PhD Thesis. University Munich, Germany.
Dalton, P., Doolittle, N., Nagata, H., & Breslin, P. (2000).
The merging of the senses: integration of subthreshold taste and smell.
Nature neuroscience, 3(5), 431-432.
Delwiche, J. F., & Heffelfinger, A. L. (2005).
Cross‐modal additivity of taste and smell.
Journal of Sensory Studies, 20(6), 512-525.
Eriksson, L., Byrne, T., Johansson, E., Trygg, J., & Vikström, C. (2013).
Multi-and megavariate data analysis basic principles and applications (Vol. 1). Umetrics Academy.
Farah, A. (2019). Coffee: Production, quality and chemistry. Royal society of chemistry.
Frank, O., Blumberg, S., Kunert, C., Zehentbauer, G., & Hofmann, T. (2007).
Structure determination and sensory analysis of bitter-tasting 4-vinylcatechol oligomers and their identification in roasted coffee by means of LC-MS/MS.
Journal of Agricultural and Food Chemistry, 55(5), 1945-1954.
Frank, O., Zehentbauer, G., & Hofmann, T. (2006).
Bioresponse-guided decomposition of roast coffee beverage and identification of key bitter taste compounds.
European Food Research and Technology, 222(5), 492-508.
Galindo‐Prieto, B., Eriksson, L., & Trygg, J. (2014).
Variable influence on projection (VIP) for orthogonal projections to latent structures (OPLS).
Journal of Chemometrics, 28(8), 623-632.
Gao, C., Tello, E., & Peterson, D. G. (2021).
Identification of coffee compounds that suppress bitterness of brew.
Food Chemistry, 350, 129225.
Ginz, M., & Engelhardt, U. H. (2000).
Identification of proline-based diketopiperazines in roasted coffee.
Journal of Agricultural and Food Chemistry, 48(8), 3528-3532.
ICO. (2019). International Coffee Organization - Coffee Market Report.
Retrieved from ICO Coffee Market Report, https://www.ico.org/documents
Kreppenhofer, S., Frank, O., & Hofmann, T. (2011).
Identification of (furan-2-yl) methylated benzene diols and triols as a novel class of bitter compounds in roasted coffee.
Food Chemistry, 126(2), 441-449.
Lang, R., Klade, S., Beusch, A., Dunkel, A., & Hofmann, T. (2015).
Mozambioside is an arabica-specific bitter-tasting furokaurane glucoside in coffee beans.
Journal of Agricultural and Food Chemistry, 63(48), 10492-10499.
Lioe, H. N., Apriyantono, A., Takara, K., Wada, K., & Yasuda, M. (2005).
Umami taste enhancement of MSG/NaCl mixtures by Subthreshold L‐α‐aromatic amino acids.
Journal of Food Science, 70(7), s401-s405.
Meyerhof, W. (2005).
Elucidation of mammalian bitter taste.
Reviews of physiology, biochemistry and pharmacology, 37-72.
Meyerhof, W., Batram, C., Kuhn, C., Brockhoff, A., Chudoba, E., Bufe, B., Appendino, G., & Behrens, M. (2010).
The molecular receptive ranges of human TAS2R bitter taste receptors.
Chemical senses, 35(2), 157-170.
Miyazawa, T., Gallagher, M., Preti, G., & Wise, P. M. (2008).
The impact of subthreshold carboxylic acids on the odor intensity of suprathreshold flavor compounds.
Chemosensory Perception, 1(3), 163-167.
Nehlig, A., Daval, J.-L., & Debry, G. (1992).
Caffeine and the central nervous system: mechanisms of action, biochemical, metabolic and psychostimulant effects.
Brain Research Reviews, 17(2), 139-170.
Nijssen, L. (1996).
Volatile Compounds in Food: Qualitative and Quantitative Data . TNO Nutrition and Food Research Institute.
In: Centraal Instituut voor Voedingsonderzoek: Zeist, The Netherlands.
Richter, H., & Spiteller, G. (1978).
Über ein neues Atractyligenin‐Glycosid aus grünen Kaffeebohnen. Chemische Berichte, 111(10), 3506-3509.
Ronningen, I., Miller, M., Xia, Y., & Peterson, D. G. (2017).
Identification and validation of sensory-active compounds from data-driven research: a flavoromics approach.
Journal of Agricultural and Food Chemistry, 66(10), 2473-2479.
Saison, D., De Schutter, D. P., Uyttenhove, B., Delvaux, F., & Delvaux, F. R. (2009).
Contribution of staling compounds to the aged flavour of lager beer by studying their flavour thresholds.
Food Chemistry, 114(4), 1206-1215.
Schwartz, T. W., & Holst, B. (2007).
Allosteric enhancers, allosteric agonists and ago-allosteric modulators: where do they bind and how do they act?
Trends in pharmacological sciences, 28(8), 366-373.
Semmelroch, P., & Grosch, W. (1996).
Studies on character impact odorants of coffee brews.
Journal of Agricultural and Food Chemistry, 44(2), 537-543.
Semmelroch, P., Laskawy, G., Blank, I., & Grosch, W. (1995).
Determination of potent odourants in roasted coffee by stable isotope dilution assays.
Flavour and fragrance journal, 10(1), 1-7.
Shibamoto, T., Harada, K., Mihara, S., Nishimura, K., Yamaguchi, K., Aitoku, A., & Fukada, T. (2012).
Application of HPLC for evaluation of coffee flavor quality.
Quality of Foods and Beverages: Chemistry and Technology, 2, 311-334.
Sittipod, S., Schwartz, E., Paravisini, L., & Peterson, D. G. (2019).
Identification of flavor modulating compounds that positively impact coffee quality.
Food Chemistry, 301, 125250.
Sittipod, S., Schwartz, E., Paravisini, L., Tello, E., & Peterson, D. G. (2020).
Identification of Compounds that Negatively Impact Coffee Flavor Quality Using Untargeted Liquid Chromatography/Mass Spectrometry Analysis. Journal of Agricultural and Food Chemistry, 68(38), 10424-10431.
Stark, T., & Hofmann, T. (2005).
Structures, sensory activity, and dose/response functions of 2, 5-diketopiperazines in roasted cocoa nibs (Theobroma cacao).
Journal of Agricultural and Food Chemistry, 53(18), 7222-7231.
Sterckx, F. L., Missiaen, J., Saison, D., & Delvaux, F. R. (2011).
Contribution of monophenols to beer flavour based on flavour thresholds, interactions and recombination experiments.
Food Chemistry, 126(4), 1679-1685.
Stevens, J. C. (1997).
Detection of very complex taste mixtures: generous integration across constituent compounds.
Physiology & behavior, 62(5), 1137-1143.
Wold, S., Sjöström, M., & Eriksson, L. (2001).
PLS-regression: a basic tool of chemometrics.
Chemometrics and intelligent laboratory systems, 58(2), 109-130.
