
ABSTRACT
- Coffee roasting 동안의 쓴맛 나는 전구물질들(bitter precursors)인
┌ 3-O-caffeoyl quinic acid (1),
├ 5-O-caffeoyl quinic acid (2), and
└ 4-O-caffeoyl quinic acid (3)의 분해 뿐만 아니라
bitter tastants의 형성에 대한 roasting time과 temperature의 영향을 탐구하기 위해, 우리는
┌ 260 ℃에서 60-600 s 동안, 또는 --┐
└ 190-280 ℃에서 240 s 동안 -------┘로스트 된 콩들로부터 coffee brews를 마련했다. - HPLC-UV/vis and HPLC-MS/MS에 의하여,
쓴맛 나는(bitter-tasting)
┌ monocaffeoyl quinides (4~8),
├ dicaffeoyl quinides (9~11), and
├ 4-vinylcatechol oligomers (12~20) 뿐만 아니라
└ parent bitter precursors 1~3이 ⇒ 이 brews에서 정량적으로 분석되었다.
- 커피-전형적인 쓴맛 프로파일을 보이는 Quinides 4~11가
약간 medium 정도의 배전도에서 더 잘 형성되는 것으로 발견되었고,
더 강한 로스팅 조건들 하에서는
다시 또 분해하여
harsh bitter-tasting 4-vinylcatechol oligomers를 형성한다는 것이 관찰되었는데,
이는 센서리 연구들에 의해서 관찰된 bitter taste quality에서의 변화에 잘 매치되는 결과이다. - 추가적으로
water percolation 중의 ground coffee로부터의
bitter compounds의 발산 프로파일에 관한 정량적 연구는
⇒ compounds 1~8은 빠르게 추출되었고(rapidly extracted)
⇒ dicaffeoyl quinides 9~11는 다소 천천히 발산되었으며,
⇒ compounds 12~17은 ground coffee material에의 강한 유지(strong retention)를 보이는 것이
발견되었음을 나타냈다. - 이 데이터는
roasting 및 extraction 조건들에 대한 지식-기반 컨트롤이
커피 음료의 쓴맛 시그니쳐(bitter taste signature)를 조절하는데 도움이 될 수도 있음을 시사한다.
INTRODUCTION
- Coffee roasting 동안의 Freshly brewed coffee는 전세계적으로
┌ 그 stimulating effect,
├ attractive aroma, 그리고
└ 쓴맛과 신맛 중심의 독특한 맛 때문에 - 소비자들에 의해 높이 평가된다. - ┌ gas chromatography와 olfactometry에 의한
│ 커피 휘발성물질들의 odor activity에 대한 screening과,
├ 안정적인 isotope dilution analyses를 사용한 most odor-active molecules의 정량화, 그리고
└ aroma reconstitution 실험들이
⇒ 1,000가지 휘발성 물질들 중 단 ~25가지만이
신선하게 마련된 커피 음료의 전반적인 아로마에 공헌한다는 것을 인상적으로 보였다 [1-4]. - 반대로, 커피 음료의 전형적인 쓴맛을 유도하는 분자들에 대한 지식은 여전히 포괄적이지 않다.
- 지난 30년 동안에 걸쳐 수행된 일련의 연구들은 커피 내의 쓴맛 분자들의 식별에 초점을 맞췄고
┌ 알칼로이드(alkaloids) caffeine과 trigonelline [5] 뿐만 아니라, 예를 들어,
├ furfuryl alcohol [6],
├ 5-hydroxymethyl-2-furanaldehyde [7],
├ pyrazines [7], and
└ diketopiperazines [8]와 같은 열에 의해 생성되는 화합물들을
⇒ 핵심적인 쓴맛 화합물들의 추정적 후보들로 제시했다. - 그러나,
┌ 커피 음료에 대한 systematic sensory-guided fractionation 뿐만 아니라
└ LC-MS/MS 및 one- and two-dimensional NMR 스터디들이 수반되는
suitable model systems이
⇒ 커피 로스팅 동안에….생두의 주요 폴리페놀들인
┌ 3-O-caffeoyl quinic acid (1),
├ 5-O-caffeoyl quinic acid (2), and
└ 4-O-caffeoyl quinic acid (3)이 각각
⇒ bitter-tasting caffeoyl quinic acid lactones (Figure 1)
┌ 5-O-caffeoyl-muco-γ-quinide (4),
├ 3-O-caffeoyl-γ-quinide (5),
├ 4-O-caffeoyl-muco-γ-quinide (6),
├ 5-O-caffeoyl-epi-δ-quinide (7),
├ 4-O-caffeoyl-γ-quinide (8),
├ 3,4-O-dicaffeoyl-γ-quinide (9),
├ 4,5-O-dicaffeoyl-muco-γ-quinide (10), and
└ 3,5-O-dicaffeoyl-epi-δ-quinide (11)로
열 변환 된다(thermally transformed)는 것을 밝혔다 [9]. - 나아가
일련의 lingering and harsh bitter-tasting 4-vinylcatechol oligomers (12-20, Figure 1)이
최근에 커피 음료에서 식별되었고
┌ 5-O-caffeoyl quinic acid (2, Figure 1)와
└ caffeic acid의 열분해(thermal degradation) 동안에 형성된다는 것이 밝혀졌다 [10, 11] - 비록 어떤 예비 데이터가
커피 콩들의 로스팅 동안에 O-caffeoyl quinic acids의 분해에 관해 보고된 바 있지만 [12-16],
┌ bitter-tasting caffeoyl quinides 4-11과
└ harsh bitter-tasting 4-vinylcatechol oligomers 12-20에 대한
로스팅 파라미터들의 영향에 관한 체계적 연구들은 부족하다. - 본 연구의 목적은, 그러므로,
roasting degree가 다른 커피 콩들로 신선하게 마련된 음료 내의
┌ bitter-tasting ┌ O-caffeoyl quinides 4-11 and
│ └ 4-vinylcatechol oligomers 12-20 뿐만 아니라
└ parent O-monocaffeoyl quinic acids 1-3의
양을 정량적으로 결정하는 것이었다.
또한 hot water percolation 동안의 이 화합물들의 발산이 정량적 토대 위에서 탐구 되어야 한다.

MATERIALS AND METHODS
Chemicals.
- 다음의 화합물들이 상업적으로 구입되었다 :
- D-(-)-quinic acid (퀸산),
p-toluenesulfonic acid monohydrate (p-톨루엔 술폰산 수화물),
chloro formic acid 2,2,2-trichloroethyl ester (크로로포름산 2,2,2-트리크로로에틸 에스테르),
anhydrous pyridine (무수 피리딘),
caffeic acid (커피산),
methyl chloro-formate (메틸 크로로포름),
ammonium formate (포름산 암모늄),
5-O-caffeoyl quinic acid (5-O-카페욜 퀴닉산, 5-CQA, 클로로제닉산),
resveratrol (레스베라트롤) (Sigma Aldrich, Steinheim, Germany), - sodium hydrogen carbonate (탄산수소나트륨),
hydrochloric acid (염산),
sodium sulfate (황산나트륨),
trichloroacetic acid (삼염화초산),
sodium hydroxide (수산화나트륨, 가성소다),
thionyl chloride (염화 티오닐),
lithium chloride (염화 리튬),
sodium carbonate (탄산나트륨), - sodium chloride (염화나트륨) (Merck, Darmstadt, Germany),
- formic acid (포름산, 개미산) (Grüssing, Filsum, Germany), and
- d4-methanol (Euriso-Top, Saarbrücken, Germany).
- Solvents는 HPLC grade의 것들이었다 (Merck).
- 최근에 보고된 프로토콜[9]에 따라서,
3-O-caffeoyl quinic acid (1),
5-O-caffeoyl quinic acid (2),
4-O-caffeoyl quinic acid (3),
5-O-caffeoyl-muco-γ-quinide (4),
3-O-caffeoyl-γ-quinide (5),
4-O-caffeoyl-muco-γ-quinide (6),
5-O-caffeoyl-epi-δ-quinide (7), and
4-O-caffeoyl-γ-quinide (8)이
decaffeinated coffee 또는 열처리된 5-O-caffeoyl quinic acid으로부터
분리되어 정제되었다.
- 4,5-O-Dicaffeoyl-muco-γ-quinide (10) and
3,5-O-dicaffeoyl-epi-δ-quinide (11)는
열처리된
┌ 4,5-O-dicaffeoyl quinic acid and
└ 3,5-O-dicaffeoyl quinic acid 로부터 각각 분리되었다 [9]. - 커피 콩들(Arabica Brazil, Santos)은 커피 업계에 의해서 제공되었다.
Preparation of a Standard Coffee Beverage.
- 커피 콩들이 a batch mill (IKA, Staufen, Germany)로 분쇄된 후에,
커피 파우더 aliquots (54 g)을 커피 필터(No. 4, Melitta)에 넣고, 여과물이 1.0 L의 부피가 될 때까지
끓는 물로 퍼콜레이트 되었다. - 그렇게 얻어진 커피 음료는 얼음 통에서 즉시 상온까지 냉각되었다.
Sequential Hot Water Extraction of Ground Coffee.
- 분쇄 커피 Aliquots (5.4 g)을
⇒ 빈 고체상 추출관(solid-phase extraction tube)에 넣고(Phenomenex, Aschaffenburg, Germany)
(volume of 60 mL),
⇒ 필터 페이퍼 디스크로 막았으며,
⇒ 고체상 추출 진공 처리기(solid-phase extraction vacuum processor) (Phenomenex)를 사용하여
10개의 aliquots (10 mL each)에서 끓는 물로 순차적으로 퍼콜레이트하였다. - 그 10개의 용출 단계들 각각의 여과물들(filtrates)은 따로 따로따로 부피 측정 플라스크에 수거되었다.
- 추가적으로, 커피 파우더 aliquots (5.4 g)을
⇒ 고체상 추출관(a solid-phase extraction tube)에 넣고
⇒ 열수(100 mL)로 퍼콜레이트 했고
⇒ 그 용출물(effluent)은 얼음 냉각된 유리병(ice-cooled glass vial)에 수거되었다.
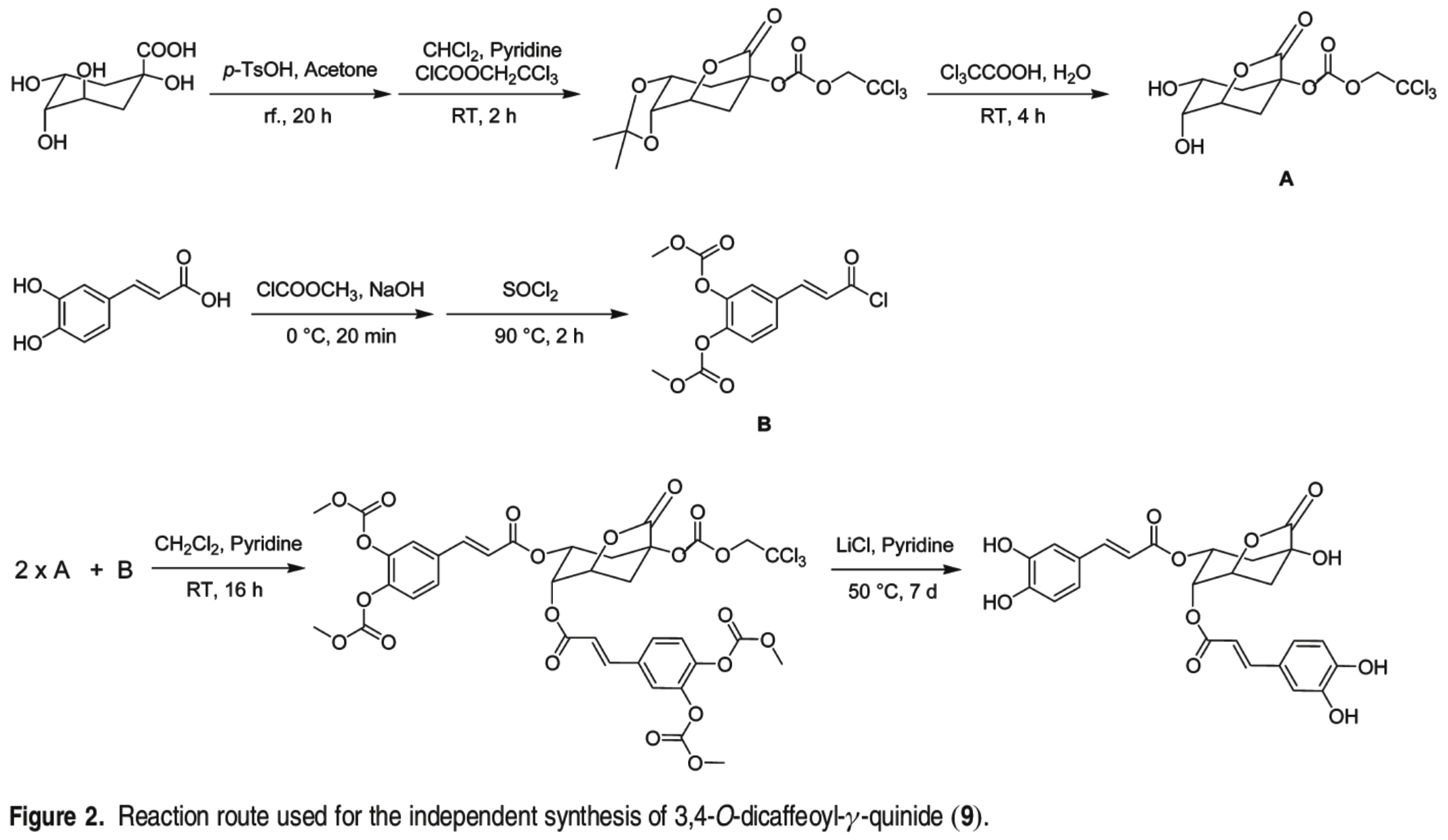
Synthesis of 3,4-O-Dicaffeoyl-γ-quinide (9).
- 문헌[17]에 나온 절차에 따라 일부 수정하여,
D-(-)-quinic acid (156 mmol)와
p-toluenesulfonic acid monohydrate (5.89 mmol)를
⇒ dry acetone (600 mL)에 suspend하였고,
⇒ Soxhleth apparatus에서 20 h 동안 reflux(환류)하였는데,
여기에는 분자 체(molecular sieve) [15 g, 4 Å (Merck)]로 채워진
추출 골무(extraction thimble)가 장착되어져 있었다. - 샘플이 5 ℃까지로 냉각된 후에,
sodium hydrogen carbonate (95.2 mmol)이 더해졌고,
그 현탁액이 추가로 60 min 동안 저어졌다. - Filtration 후에,
⇒ 그 솔벤트는 진공에서 제거되었고,
⇒ 나머지는 dichloromethane (300 mL)에 넣어졌고
⇒ 3,4-O-isopropyliden-1,5-quinide가 n-hexane (300 mL)의 추가 중에 결정화되었다. - chloroformic acid 2,2,2-trichloroethyl ester (156 mmol) in dichloromethane (50 mL)의 용액이
3,4-O-isopropyliden-1,5-quinide (146 mmol),
pyridine (338 mmol), 그리고
dichloro-methane (300 mL) 혼합물로 0 ℃에서 적상으로(dropwise) 더해졌고,
그런 다음, 상온에서 2 h 동안 저어졌다. - 형성된 백색의 침전물이
⇒ filtration에 의해 분리되어
⇒ dichloromethane (400 mL)에 용해되었고,
⇒ 그 용액은 hydrochloric acid (1 mol/L, 2×150 mL)으로 그리고 그 다음에
⇒ water (100 mL)에 의해서 추출되었다. - 그 유기층이 Na2SO4(황산나트륨)로 건조되었고,
- 그 다음에 진공에서 100 mL까지로 농축되었으며,
- ethanol (800 mL)을 추가하여 밤새도록 4 ℃에서 냉각되어
- 1-O-(2,2,2-trichloroethoxycarbonyl)-3,4-O-isopropyliden-1,5-quinide가
침전되어 filtration으로 분리되었다. - Water (6.8 mL)가 trichloroacetic acid (374 mmol)에 더해진 다음,
맑은 용액이 얻어질 때까지 가열되었고
그 샘플이 상온까지 식은 후에,
1-O-(2,2,2-trichloroethoxycarbonyl)-3,4-O-isopropyliden-1,5-quinide (118 mmol)이
비율에 따라 더해졌다. - 그 샘플을 4 h 동안 저은 후에,
⇒ ice-cooled water (450 mL), ethylacetate (900 mL), 그리고 그 다음에
aqueous NaHCO3 solution (405 mmol in 900 mL of water)이
차례로 그 반응 혼합물이 더해졌다.
⇒ 그 유기상(organic phase)이 분리되어
⇒ aqueous NaHCO3 solution (2% in water, 120 mL)과 water (120 mL)로 추출되었다. - 그 유기층이 Na2SO4로 건조되었고
그 솔벤트가 진공에서 제거되었으며
나머지가 70 ℃에서 toluene (250 mL)에 용해되었다. - 그 용액은 밤새도록 4 ℃에서 유지되어
백색의 무정형의 파우더(white amorphous powder)로서
1-O-(2,2,2-trichloroethoxycarbonyl)-1,5-quinide가 침전되었으며
이것이 filtration으로 분리되어 진공에서 건조되었다. - Methyl chloroformate (9.4 mL)를
⇒ 0 ℃에서 caffeic acid (51 mmol) in aqueous NaOH (1 mol/L, 150 mL)의 용액에
적상으로(dropwise) 더했고,
⇒ 그 다음에, 노란 잔유물을 제공할 때까지 0 ℃에서 20 min 동안 저었다. - aqueous HCl (2 mol/L)으로 그 반응 혼합물을 neutralization 한 후에,
⇒ 남은 것은 filtration에 의해 분리하였다. - aqueous ethanol (50%, 250 mL)로부터의 재결정화(Recrystallization)가
⇒ 백색 결정으로서의 3,4-O-dimethoxycarbonyl caffeic acid를 제공하였다. - 3,4-O-dimethoxycarbonyl caffeic acid (14.0 mmol)에
⇒ Thionyl chloride (96.0 mmol/L)를 적상으로 더했고,
⇒ 그 현탁액을 gas 발현이 완료될 때까지 90 ℃로 가열했고
⇒ 나머지 thionyl chloride는 nitrogen gas 스트림으로 제거하였다. - toluene (150 mL)으로의 재결정화(Recrystallization)가
노르스름한 결정들로서의 3,4-O-dimethoxycarbonyl caffeic acid chloride을 제공했다.
O-(dimethoxycarbonyl)caffeoyl]-1,5-quinide.
- 3,4-O-dimethoxycarbonyl caffeic acid chloride (14.0 mmol) in dichloromethane (30 mL) 용액을
1-O-(2,2,2-trichloroethoxycarbonyl)-γ-quinide (4.21 mmol) and
pyridine (17.9 mmol) in dichloromethane (30 mL)의 용액에
0 ℃에서 적상으로 더했다. - 그 혼합물을 밤새 저은 후에,
⇒ 그 솔벤트는 진공에서 제거되었고,
⇒ 나머지는 ethyl acetate (200 mL)에 용해했으며
⇒ 그 다음에 aqueous HCl solution (1 mol/L, 35 mL),
an aqueous NaHCO3 solution (2%, 35 mL), 그리고
water (35 mL)로 순차적으로 추출하였다. - 그 유기층은 Na2SO4로 건조되었고,
⇒ 솔벤트는 진공에서 분리되어
⇒ 순수한
1-O-(2,2,2-trichloroethoxycarbonyl)-3,4-bis[3,4-O-(dimethoxycarbonyl)caffeoyl]-1,5-quinide를
만들었다. - 이 산물의 앨리컷(2.21 mmol)을
⇒ lithium chloride (23.6 mmol) in pyridine (20 mL)으로 suspend 했고
⇒ 그 다음에 50 ℃에서 7일 동안 저었다. - 그 솔벤트가 진공에서 제거된 후에,
⇒ 그 나머지는 ethyl acetate (100 mL)에 용해되었고,
⇒ 그 용액은 an aqueous HCl solution (1 mol/L, 50 mL),
an aqueous Na2CO3 solution (2%, 50 mL), 그리고
brine (50 mL)으로 순차적으로 추출되었다. - Na2SO4로의 유기층 건조와 진공에서의 솔벤트 분리는
⇒ 갈색의 잔유물을 제공하였는데,
⇒ 이것이
an ethyl acetate/methanol mixture (80/20, v/v)에 맞춰진(conditioned)
Polyamide MN-SC-6 material (Macherey-Nagel, Düren, Germany)의 슬러리로 채워진
a glass column (300 mm × 30 mm)의 상부에 적용되었다(applied). - 그 컬럼을
⇒ ethyl acetate/methanol mixture (80/20, v/v) (500 mL)로 헹군 다음,
⇒ methanol의 양을 늘려 (from 30 to 100%)
ethyl acetate/methanol mixtures (300 mL each)로 헹구었다. - 진공에서의 솔벤트 분리 후에,
⇒ 70/30 (v/v) 그리고 60/40 (v/v) ethyl acetate/methanol 혼합물이
표적 화합물인 3,4-O-dicaffeoyl-γ-quinide를 제공했는데,
⇒ 이는 열처리된 3,4-O-dicaffeoyl-γ-quinic acid [9]로부터 분리되어진
3,4-O-dicaffeoyl-γ-quinide에 대해 최근에 보고된 것의
chromatographic (RP-HPLC) and spectroscopic data (LC-MS/MS, NMR, and UV/vis)의
비교로 그 identity가 확인되었다.
3,4-O-Dicaffeoyl-γ-quinide (9)
(the arbitrary numbering of the carbon atoms refers to the structure in Figure 2) :
UV/vis [5/5 (v/v) methanol/ water] λmax = 235, 300, 328 nm;
LC-MS (ESI-) m/z 497 (100; [M - H]-);
1H NMR (400 MHz, d3-MeOD, COSY) δ 2.20-2.34 [m, 2H, H-C(2eq), H-C(2ax)],
2.45-2.62 [m, 2H, H-C(6eq), H-C(6ax)],
4.95 [dd, 1H, J = 5.6, 5.0 Hz, H-C(5eq)],
5.20 [ddd, 1H, J = 11.5, 6.6, 4.7 Hz, H-C(3ax)],
5.63 [dd, 1H, J = 4.7, 5.0 Hz, H-C(4eq)],
6.16 [d, 1H, J = 15.9 Hz, H-C(5’)],
6.40 [d, 1H, J = 15.7 Hz, H-C(5”)],
6.70 [d, 1H, J = 8.1 Hz, H-C(3’)],
6.81 [d, 1H, J = 8.2 Hz, H-C(3”)],
6.83 [dd, 1H, J = 8.1, 2.1 Hz, H-C(2’)],
6.99 [dd, 1H, J = 8.2, 2.1 Hz, H-C(2”)],
7.02 [d, 1H, J = 2.1 Hz, H-C(1’)],
7.10 [d, 1H, J = 2.1 Hz, H-C(1”)],
7.50 [d, 1H, J = 15.9 Hz, H-C(4’)],
7.64 [d, 1H, J = 15.7 Hz, H-C(4”)].
Quantitative Analysis of
O-Caffeoyl Quinic Acids 1-3 and O-Caffeoyl-Quinides 4-8.
- 표준 커피 음료의 분취물들(10 μL)을
페닐헥실 루나(Phenyl-hexyl Luna), 250 mm × 4.6 mm(내경), 5 μm 컬럼 (Phenomenex)을 이용하여
HPLC-UV/vis 분석하였다. - 이때 메탄올(solvent A)의 gradient를 사용했고, 그리고
포름산 암모늄 수용액 buffer (0.25 mol/L, pH 3.5, solvent B)을 이동상(mobile phase)으로 사용했다. - Chromatography는
Solvent A 25% 농도로 시작하여, 0.8 mL/min의 유속으로 진행하였고,
이후 solvent A의 함량을 38분 이내에 28%까지 증가시킨 후,
6.5분 이내에 100%까지 증가시키고,
마지막으로 용매 A 100% 농도를 5분 더 유지하였다. - 레퍼런스 화합물들에 대해 얻어진 데이터와
분석물들의 크로마토그래픽 데이터 (retention time) 및
스펙트로스코픽 데이터 (UV/vis and LC-MS/MS)를 비교하여, - 3-O-caffeoyl quinic acid (1),
5-O-caffeoyl quinic acid (2),
4-O-caffeoyl quinic acid (3),
5-O-caffeoyl-muco-γ-quinide (4),
3-O-caffeoyl-γ-quinide (5),
4-O-caffeoyl-muco-γ-quinide (6),
5-O-caffeoyl-epi-δ-quinide (7), and
4-O-caffeoyl-γ-quinide (8)를 식별한 후에, - 324 nm에서 얻어진 피크 에리어와
메탄올/물 혼합물 (pH 3.5) 내의 5-O-caffeoyl quinic acid 1/1 (v/v) 정의된 스탠다드 용액들의 것들을 비교하여,
정량화가 수행되었다.
Quantitative Analysis of O-Dicaffeoyl-Quinides 9~11.
- 스탠다드 커피 음료의 분취물들(aliquots) (10 μL)의 분석은 다음 방법들을 사용해서 이뤄졌다.
LC-MS/ MS
⇒ RP-18 Synergi Fusion에서 negative ionization mode로 작동.
⇒ 컬럼 = 150 mm × 2.0 mm (inside diameter), 5 μm column (Phenomenex)
⇒ gradient = 메탄올 (solvent A)와 0.1% 포름산 수용액 (solvent B), 유속 = 0.25 mL/min. - 우리는 solvent A의 함량을 15분 동안 40%에서 60%까지 증가시키고,
그 다음에 25분 내에 solvent A 함량은 100%까지 증가시킨 후,
마지막으로 추가 5분 동안 100% solvent A를 유지하여 크로마토그래피를 수행했다. - 3,4-O-dicaffeoyl-γ-quinide (9),
4,5-O-dicaffeoyl-muco-γ- quinide (10), and
3,5-O-dicaffeoyl-epi-δ-quinide (11)의 식별을,
이 물질들의 크로마토그래픽 데이터 (retention time)와 스펙트로스코픽 (LC-MS/MS) 데이터와
메탄올과 0.1% 포름산 수용액의 혼합물 (1/1, v/v)에 용해된
합성 3,4-dicaffeoyl-γ-quinide의 규정된 스탠다드 용액들의 데이터와 비교하여 수행하였다. - multiple-reaction monitoring (MRM) mode를 사용하여,
타겟 퀴니드들 9 (m/z 497.0 → 335.0), 10 (m/z 497.0 → 335.0), and 11 (m/z 497.0 → 335.0)이
괄호들에 주어진 mass transitions를 사용하여 분석되었다 (Figure 3).

Quantitative Analysis of 4-Vinylcatechol Oligomers.
- 표준 커피 음료의 분취물들(Aliquots) (900 μL)을
⇒ 염산(hydrochloric acid) (50 μL)을 이용해 pH 2로 산성화한 다음,
⇒ 내부 표준인 레스베라트롤(resveratrol) (50 μL, 2.5 μg/mL) 용액과 함께
1/1(v/v) 메탄올/물 혼합물(pH 3.5)에 섞었다 (spiked). - 그 샘플들의 균질화 후에, 분취물들 (20 μL)이 다음 방법에 의해 분석되었다.
- HPLC-MS/MS
⇒ Zorbax Eclipse XDB C18 컬럼, negative ionization mode로 작동 ,
150 mm × 2.1 mm (inside diameter), 5 μm column (Agilent, Waldbronn, Germany)
⇒ 다음과 같은 괄호들 속에 주어진 mass transitions로 MRM mode를 사용하여 분석.
⇒ resveratrol (m/z 227.0 → 143.1),
12 (m/z 271.0 → 109.0), 13 (m/z 271.0 → 109.0), 14 (m/z 271.1 → 109.0),
15 (m/z 273.2 → 109.0), 16 (m/z 271.1 → 109.1), 17 (m/z 271.1 → 109.1),
18 (m/z 407.1 → 297.2), 19 (m/z 407.1 → 297.2), and 20 (m/z 407.2 → 161.2).

- Chromatography는 다음과 같은 gradient로 수행.
⇒ acetonitrile (solvent A) 그리고 0.1% 포름산 수용액 (solvent B), flow rate는 0.25 mL/min.
⇒ 솔벤트 A 25%로 시작하여,
5분 내에 솔벤트 A의 함량을 28%로 올리고,
그 다음 20분 내에 30%까지,
그 다음 5분 내에 100%로 올린 다음,
마지막으로 추가 2분 동안 100%에서 유지. - 타겟 화합물들 12~20이 내부 스탠다드로서 레스베라트롤(resveratrol)을 거쳐 정량화되었음.
- 개별 4-vinylcatechol oligomers의 농도들은
⇒ 분석물 대 내부 스탠다드의 피크 에리어 비율들을
각 분석물 대 내부 스탠다드의 농도 비율들 (0.3~3)에 대해 plotting을 하여
선형회귀분석(linear regression)을 사용하여 만든
보정 곡선(calibration curves)을 사용하여 계산되었음.
High-Performance Liquid Chromatography (HPLC)..
- HPLC 장비 (Agilent)의 구성
a series HP 1050-type quaternary pump system,
an HP 79855 A/B-type autosampler, and
a MWD 79854 A-type multiwavelength detector.

High-Performance Liquid Chromatography with Tandem Mass Spectrometry (HPLC-MS/MS).
- The Agilent 1100 Series HPLC system의 구성 : a pump, a degasser, and an autosampler (Agilent)
- 다음 장비에 연결하여 사용.
a 4000 QTrap triple quadrupole/linear ion trap mass spectrometer
(Applied Biosystems/MDS Sciex, Darmstadt, Germany)
with an electrospray ionization (ESI) device running in negative ionization mode
with a spray voltage of -4500 V.
Nitrogen ⇒ curtain (20 psi), nebulizer (35 psi), and heater (45 psi) gas로 적용.
Detection ⇒ the multiple-reaction monitoring (MRM) mode로 수행되었음, - negative pseudomolecular ion [M-H]- 로부터
collision-induced dissociation 후에 생성된 main fragment로의 transition을 기록. - The quadrupoles ⇒ unit mass resolution에서 작동.
- 소프트웨어 Sciex Analyst (version 1.4.1) ⇒ 장비 컨트롤 및 데이터 분석을 위해 사용.

Sensory Analyses..
General Conditions and Panel Training.
- 12명의 평가자들 (남성 5인, 여성 7인, 22~40세), 본 연구의 센서리 테스트 참가 동의를 받음.
- 알려진 미각 장애 병력은 없었음.
- 적어도 2년 동안 앞서 설명된 바와 같이 [18-21] 주단위의 트레이닝 세션들에서 훈련 받았고,
따라서 적용되는 이 테크닉에 친숙했음. - 센서리 분석들은 22℃에서 공조시설이 설치된 분리된 부쓰들이 있는 룸에서 수행되었고,
3회의 독립적 세션들로 이뤄졌다. - 후각 반응들과의 교차-모달 상호작용을 방지하기 위해, 패널리리스트들은 코 클립을 사용했다.
Bitter Taste Analysis.
- 갓 마련된 커피 음료들이 센서리 분석을 위해 사용되었다.
- 센서리 패널리스트들에게 샘플들(5 mL)을 제시하여,
0 (not detectable)에서부터 10.0 (strong taste impression)까지의 스케일 상에서
┌ bitter taste intensity
└ bitter quality를 채점해달라고 요청하였다
RESULTS AND DISCUSSION
- 최근 탐구들이
monocaffeoyl quinic acid lactones 4-8 (Figure 1),
dicaffeoyl quinic acid lactones 9-11,
4-vinylcatechol dimers 12-17, 그리고
4-vinylcatechol trimers 18-20의 발견으로 이끌었고, - 이들은 모두 배전 커피의 강렬한 쓴 화합물들로서 [9, 10],
5-O-caffeoyl quinic acid (2)의 열 분해 중에 생성된다. - 로스트 커피에서의 Bitter taste 발현 뿐만 아니라
이 bitter compounds의 생성에 대한 로스팅 파라미터들의 영향을 탐구하기 위해서,
coffee brews의 bitter tastants 4-20 뿐만 아니라
그들의 parent monocaffeoyl quinic acids 1-3에 대한 정량적 분석을 위해 분석 절차들이 개발되었다.
Quantitative Analysis of Compounds 1-20 in Coffee Brew.
- monocaffeoyl quinic acids (1-3)와 monocaffeoyl quinides (4-8)에 대한 정량적 분석을 위해,
갓 분쇄된 배전커피의 샘플들을 뜨거운 물로 퍼콜레이팅함으로써 마련된 coffee brews가
고정상(stationary phase)으로서 Phenylhexyl material를 사용하여
HPLC-UV/vis에 의해 직접적으로 분석되었다. - 예비 연구들이
┌ monocaffeoyl quinic acids와
└ corresponding quinides의 경우에 동일한 소멸계수를 보였기 떄문에
⇒ 5-O-caffeoyl quinic acid가 compounds 1-8의 정량화를 위한 외부적 스탠다드로서 사용되었다. - Coffee brew 내의 Dicaffeoyl-quinides
┌ 3,4-O-dicaffeoyl-γ-quinide (9),
├ 4,5-O-dicaffeoyl-muco-γ-quinide (10), and
└ 3,5-O-dicaffeoyl-epi-δ-quinide (11)에 대한 분석이
⇒ RP18-HPLC-MS/MS running in the multiple-reaction monitoring (MRM) mode에 의해서
성공적으로 이뤄졌다 (Figure 3).

- bitter compounds 9-11의 정량적 결정은
┌ corresponding mass transition의 trace의 경우에 얻어진 peak area와
└ Figure 2에서 주어진 multistep synthesis에서 quinic acid와 caffeic acid로부터 마련된
purified 3,4-O-dicaffeoyl-γ-quinide의 정의된 스탠다드 용액들의 그것들과
비교함으로써 수행되었다. - 예비 스터디들이
4-vinylcatechol oligomers 12-20가
coffee beverages의 pH value (pH 4.9-6.5)에서 다소 불안정하고
더 산성인 조건들에서 비교적 안정적이라는 것을 보였기 때문에
⇒ 갓 마련된 coffee brews의 앨리퀏들이
⇒ 염산수(aqueous hydrochloric acid)로 pH 2.0까지 산성화되었고
⇒ 그 다음에 4-vinylcatechol oligomers 12-20의 mass transitions에 대한 모니터링을 위해
RP18-HPLC-MS/MS system로 직접 주입되었다 (Figure 4). - 정량적 분석을 위해,
타겟 분석물질과 유사한 안정성 및 이온화 행태를 보이는 레스베라톨(resveratrol)이
internal standard로 사용되었다.

Influence of the Roast Gas Temperature on
the Bitterness and Concentration of 1-20 in Coffee Brew.
- 커피 콩 로스팅 동안의 쓴맛 화합물의 형성에 대한 로스트 가스 온도의 영향을 탐구하기 위해,
coffee brews가 190-280 ℃에서 240 s의 일정한 시간 동안 로스트 된 분쇄 커피 콩들로부터 신선하게 마련되었다. - 먼저, 훈련된 센서리 패널에 의하여 이 커피 음료들의 쓴맛 강도가
0 (not detectable) 부터 10 (intense bitterness) 까지의 스케일에서 관능적으로 평가되었다. - 이 스터디들은
190-210 ℃에서 240 s 동안 로스트 된 커피 샘플들은 어떠한 bitterness도 부여하지 않았음을 보였다 (Table 1). - roast gas temperature를 220 ℃에서 280 ℃로 증가하니
coffee brews의 perceived bitterness가 0.25 → 8.0으로 강한 증가를 유도했다 (Table 1).

- 가장 흥미로운 것은,
적용되는 roast gas temperature에 따라
⇒ taste intensity에서의 증가 뿐만 아니라
⇒ quality of the bitter taste에서의 변화도 관찰되었다는 것이다. - 240 ℃ 이상의 gas temperature가 커피 로스팅에 적용되었을 때,
⇒ 더 마일드하게 로스트 된 커피들의 pleasant, typical coffee-like bitterness이
특히 혀의 뒷부분과 목에서 지각되는
harsh, burnt, long-lasting, 그리고 espresso-like bitter taste modality(맛 양상)으로 변했다. - Bitter compounds 중에서 어떤 쓴 화합물들이
roast gas temperature 증가와 함께 bitter taste profile에서의 변화에 공헌할 수도 있는지를 탐구하기 위해
우리는 각 커피 샘플로부터 마련된 coffee brews 내의
┌ bitter compounds 4-20 뿐만 아니라
└ parent monocaffeoyl quinic acids (1-3)를
HPLC-UV/vis (1-8) and HPLC-MS/MS (9-20)에 의해 정량적으로 평가하였다 (Figure 5).

- 정량적 스터디들의 결과,
- 190 ℃에서 240 s 동안 로스트 된 커피 내의 지배적인 폴리페놀들로서
⇒ non-bitter 5-O-caffeoyl quinic acid (1), 그 다음이
⇒ 4-O-caffeoyl quinic acid (2)와
3-O-caffeoyl quinic acid (3)이 나타났다 (Figure 5A).
⇒ 비교해보면, bitter compounds 4-20는 미량만이 검출가능했는데,
이는 그 커피 샘플 내의 부족한 bitterness라는 것과 잘 맞는 결과였다 (Table 1). - Roast gas temperature의 증가는
monocaffeoyl quinic acids의 rapid degradation을 유도했다 ;
⇒ e.g., 190 → 280 ℃로의 증가는
caffeoyl quinic acids 1-3의 sum의 농도를 2274.8 → 33.0 mg/L of coffee brew로 감소시켰다. - Monocaffeoyl-quinides 4-8의 농도는
⇒ caffeoyl quinic acids의 분해와 병행하여, 로스팅 온도 증가와 함께 증가했고,
240℃에서 maximum을 거쳤다 :
⇒ e.g., bitter monocaffeoyl-quinides 4-8의 total amount는
roast gas temperature가 190 → 240 ℃로 증가했을 때 17.5 → 174.5 mg/L로 10배 증가했다. - Monocaffeoyl-quinides 중에서
3-O-caffeoyl-γ-quinide (5)와
4-O-caffeoyl-γ-quinide (8)이 양적으로 지배하는 isomers인 것으로 발견된 반면에,
5-O-caffeoyl-muco-γ-quinide (4),
4-O-caffeoyl-muco-γ-quinide (6), and
5-O-caffeoyl-epi-δ-quinide (7)의 레벨은 상당히 더 낮았다 (Figure 5B). - non-bitter monocaffeoyl quinic acids (1-3)에서
pleasant, coffee-specific bitter profile을 부여하는
monocaffeoyl-quinides로의 변환도 [9,10]
⇒ 220-240 ℃에서 240 s 동안 로스트 된 커피 샘플들의
mild and pleasant bitterness의 증가와 일치적이다 (Table 1). - 240 → 280 ℃로의 roast gas temperature의 추가적인 증가는
⇒ monocaffeoyl-quinide 함량의 감소를 유도했다 ;
⇒ e.g., 280 ℃에서의 로스팅은 190 ℃에서 만들어진 량에 비해
다소 낮은 레벨에서 quinides 4-8를 생성했다. - 이 데이터는
⇒ pleasant bitter-tasting monocaffeoyl-quinides의
thermal instability를 분명하게 보여주는 것이다. - dicaffeoyl quinic acid lactones
┌ 3,4-O-dicaffeoyl-γ-quinide (9),
├ 4,5-O-dicaffeoyl-muco-γ-quinide (10), and
└ 3,5-O-dicaffeoyl-epi-δ-quinide (11)의 concentration curve의 정량화는
⇒ monocaffeoyl-quinides 4-8의 경우에 발견된 것과
다소 유사한 temperature dependency를 나타냈다 (Figure 5C). - 3,4-O-dicaffeoyl-γ-quinide (9)는
dicaffeoyl-quinides의 total amounts의 80% 이상을 차지하는 main isomer인 것으로 발견되었다.
⇒ 190 ℃에서는, 단 3.2 mg/L의 total amount만이 dicaffeoyl-quinides의 경우에 발견되었고,
⇒ 230 ℃에서 최대 17.4 mg/L를 달린 후에
⇒ bitter compounds 9-11는 다시 분해하기 시작했고
⇒ 280 ℃에서 로스팅이 수행되었을 때에는 not detectable 했다. - 4-vinylcatechol oligomers 12-20의 concentrations은 (Figure 5D and Table 1)
⇒ caffeoyl-quinides 4-11와 대조적으로,
더 높은 roast gas temperature와 함께 계속 증가했고
250 ℃ 이상으로 로스트 된 커피 샘플들의 harsh and espresso-like bitterness 증가와 병행했다. - 기대와 같이, compound 14의 concentration은
⇒ 250 ℃에서 최대값이 되었다가 그 다음에 다시 감소했는데,
⇒ 이는 4-vinylcatechol dimers 12, 13, 16, and 17의 precursor로서 compound 14를 시사하는 것이며
⇒ 최근에 보고된 14의 cyclization를 통해
hydroxylated phenylindanes 12, 13, 16, and 17를 생성하는 것을 보여주는
형성 경로를 확인해주는 것이다. - Derivatives 18-20의 농도들은
⇒ 그것들의 detection thresholds에 있었고, 그러므로 정량적으로 결정되지 않았다.
⇒ roast gas temperature 190 → 280 ℃로의 증가는
4-vinylcatechol oligomers의 total concentration을
0 → 452.6 μg/L of coffee brew로 증가시켰다.
Influence of the Roasting Time on
the Concentration of Bitter Compounds 1-20 in Coffee Brew.
- 두 번째 세트의 실험들에서는,
- standard coffee brews가
260 ℃의 일정한 온도에서 60-600 s 동안 로스트 된 10가지 커피 샘플들로부터 마련되었고
bitter compounds 4-20과
parent caffeoyl quinic acids 1-3이
각각 HPLC-UV/vis와 HPLC-MS/MS에 의해서 분석되었다 (Figure 6).

- caffeoyl quinic acids 1-3이
roasting time이 증가되었을 때 다소 unstable한 것으로 발견되었다 ; e.g.,
⇒ 60 → 600 s까지의 로스팅 시간 증가는
caffeoyl quinic acids의 total amount를 2350.2 → 25.4 mg/L of coffee brew로
93배만큼 감소시켰다 (Figure 6A).
⇒ 240 s 후에는
이미, 대부분의 caffeoyl quinic acids이 분해되어 359.1 mg/L 만이 그 coffee brew에 존재했다. - bitter-tasting mono- and dicaffeoyl-quinides의 형성은
⇒ caffeoyl quinic acids의 함량 감소와 병행하면서,
Roasting time이 60 → 180 s로 증가 되었을 때 더 잘 이루어졌다 ; e.g.,
⇒ caffeoyl-quinides (4-8)과
dicaffeoyl-quinides (9-11)의 total amount는 각각 7배와 4배 증가되었다 (Figure 6B,C). - caffeoyl quinide 농도는
maximum을 지난 후에, 빠르게 감소되었다 ; e.g.,
⇒ 180 → 600 s로의 roasting time의 연장은
┌ monocaffeoyl-quinides 농도를 181.5 → 16.9 mg/L로
└ dicaffeoyl-quinides 농도를 5.69 → 0.10 mg/L로 감소시켰다. - 4-vinylcatechol oligomers의 정량분석 결과
⇒ compound 14 농도의 빠른 증가, 240 s 로스팅 후에 70 μg/L의 최대 레벨에 도달 (Figure 6D).
⇒ 비교하면, compounds 12, 13, 16, 17의 형성은
260 ℃에서 180 s 이상 동안 로스트 되었을 때 더 잘 형성 ; e.g.,
⇒ 이 4-vinylcatechol dimers의 total amount는 600 s 후에 3.5 → 245.3 μg/L로 증가되었다. - 이 데이터 역시 key intermediate로서 compound 14를 거치는
phenylindanes 12, 13, 16, 17의 제안된 형성 경로와 잘 들어맞는다 [10]. - compound 15의 농도는,
⇒ roasting degree와 독립적으로, 다소 낮았고,
⇒ 그 trimers 18-20이 미량으로만 검출되었다 (데이터는 제시하지 않았음.) - 얻어진 데이터는
⇒ 먼저, 커피 내 bitter-tasting compounds의 조성은
roasting time과 gas temperature에 강하게 종속적라는 것을 분명하게 보이고 있다. - monocaffeoyl- and dicaffeoyl-quinides
⇒ pleasant coffee-typical bitter taste profile을 나타내는 이들은
slight to medium 배전도에서 더 잘 형성될 수 있는 것으로 발견되었고
maximum을 거친 후에 다시 분해될 수 있다는 것이 관찰되어 앞선 문헌 결과들을 확인해준다 [12-16]. - 비교하면,
long lasting and harsh bitter-tasting 4-vinylcatechol oligomers의 형성은
더 강한 로스팅 조건들에서 더 잘 된다는 것이 발견되었다. - bitter tastants (4-17) 그룹 중에서의 분자 변화들은
⇒ 상응하는 커피 음료들에 대한 bitter taste quality perceived에 대한 배전도의 영향과
잘 들어맞는 것으로 보인다 ; e.g.,
⇒ slight to medium 로스트 된 커피는 mild, pleasant, and coffee-like bitter quality를 주는 반면
⇒ more severe 로스팅은 lingering, harsh bitter beverage를 초래한다는 것이 발견될 수 있었다.
Release of Monocaffeoyl Quinic Acids and Bitter Tastants from Ground Coffee
during Sequential Hot Water Extraction.
- Water percolation 중에 ground coffee로부터의 선정된 맛 화합물들의 발산에 대한 첫 통찰을 얻기 위해
우리는 갓 분쇄된 커피를 카트리지에 넣고 끓는 물 10 mL로 연속적으로 퍼콜레이팅하여 모델 실험을 수행했다. - 각 소획분의 용출물은 ice-cooled volumetric flasks에 수거되어
HPLC-UV/vis와 HPLC-MS/ MS에 의한
monocaffeoyl quinic acids 1-3 그리고 bitter compounds 4-17에 대한 정량분석을 위해 사용되었다. - 한 추가 실험에서,
동일한 량의 커피 파우더를 카트리지에 넣고, 단 1회 용리 단계(single elution step)에서
total amount의 water volume으로 퍼콜레이트하였다.

- caffeoyl quinic acids의 정량분석 결과
⇒ 첫 30 mL of water 내에서 1-3의 농도의 빠른 감소를 나타냈다 ; e.g.,
⇒ 첫 10 mL aliquot 내의 caffeoyl quinic acids의 total amount는 40mg이었고,
이는 caffeoyl quinic acids 총량의 56%를 차지하며,
⇒ 퍼콜레이션에 사용된 두번째 10 mL aliquot 내에서는 18 mg이었다 (Figure 7A). - 더 나중의 플랙션들은
비교적 소량의 caffeoyl quinic acids를 함유했다 ; e.g.,
⇒ <1.0 mg의 1-3이 여섯 번째 aliquot (fraction of 51-60 mL)에 존재했는데,
⇒ 이는 hot water percolation에 의해서
caffeoyl quinic acids가 coffee powder로부터 빠르게 추출되었음을 보여준다. - bitter-tasting monocaffeoyl quinides 4-8의 발산 패턴
- Lactones의 어느 정도 더 약한 polarity 때문에 기대될 수 있는
caffeoyl quinic acids의 것과 비교할 때
⇒ 비록 용리 커브가 약간 더 평평했지만,
⇒ 이 패턴은 quinic acids 1-3의 경우에 발견된 것과 다소 유사한 것으로 발견되었다 (Figure 7B). - 첫 10 mL volume은 추출된 quinides 4-8의 총량의 37%를 함유했다.
- 비교하면, dicaffeoyl-quinides의 농도들은 9-11의 총량의 18%만을 차지해,
⇒ 극성이 덜한 dicaffeoyl quinic acid lactones가
coffee powder로부터 다소 느리게 추출되었다는 강한 증거를 제시하는 것이다 (Figure 7C). - 퍼콜레이션에 사용된 마지막 10 mL volume (91-100 mL) 내의
dicaffeoyl-quinide 함량은 아직 12 μg이었는데,
⇒ 이는 첫 샘플의 농도의 35%에 달하며,
⇒ 따라서 분쇄 커피로부터의 이 부류의 bitter lactones의 다소 덜 효과적인 발산을 보여준다. - Harsh bitter-tasting 4-vinylcatechol oligomers 12-17의 quantitative analysis 결과
- Lactones의 그것과 비교할 때 다른 발산 행태를 나타냈다 (Figure 7D).
- 흥미롭게도, 얻어진 플랙션 당 compounds 12-17의 양들은
⇒ 퍼콜레이션의 첫 40 mL 내에서는 증가했고,
31-40 mL의 플랙션에서 2.5 μg라는 maximum에 도달했다.
⇒ 그런 다음, 플랙션 당 4-vinylcatechol oligomer content는
다시 퍼콜레이션에 사용된 마지막 10 mL에서는 ∼1.6 μg으로 다시 약간 감소했고,
여전히 첫 여과물(filtrate)에서 발견된 함량의 95%에 해당했다. - 이 데이터는
⇒ 4-vinylcatechol derivatives은 lactones에 비교할 때
coffee powder로부터 다소 느리게 발산되었고,
타겟 화합물들의 극성(polarity)에 병행하여 움직이는 것으로 보인다는 것을 분명하게 가리킨다.

LITERATURE CITED
(1) Blank, I.; Sen, A.; Grosch, W.
Potent odorants of the roasted powder and brew of Arabica coffee.
Z. Lebensm.-Unters. -Forsch. 1992, 195, 239–245.
(2) Semmelroch, P.; Grosch, W.
Analysis of roasted coffee powders and brews by gas chromatography-olfactometry
of headspace samples.
Lebensm.-Wiss. -Technol. 1995, 28, 310–313.
(3) Semmelroch, P.; Grosch, W.
Studies on character impact odorants of coffee brews.
J. Agric. Food Chem. 1996, 44, 537–543.
(4) Mayer, F.; Czerny, M.; Grosch, W.
Sensory study on the character impact aroma compounds of a coffee beverage.
Eur. Food Res. Technol. 2000, 211, 272–276.
(5) Chen, W. C.
Studies on the bitter taste of roasted coffee :
Relationship between structure and bitter taste of some organic compounds (in German).
Ph.D. Thesis, University of Munich, Munich, 1979.
(6) Shibamoto, T.; Harada, K.; Mihara, J.; Nishimura, K.; Yamaguchi, A.; Aitoku, A.; Fukada, T.
Application of HPLC for evaluation of coffee flavor quality.
In The Quality of Foods and Beverages; Charambous, G., Inglett, G., Eds.;
Academic Press: New York, 1981; Vol. 2, p 311.
(7) Belitz, H. D.
Taste-active substances in coffee.
International Coffee Science Association, 7th Colloquium;
ASIC Bremen: Hamburg, 1977; Vol. 24, pp 3-252.
(8) Ginz, M.; Engelhardt, U. H.
Identification of proline-based diketo- piperazines in roasted coffee.
J. Agric. Food Chem. 2000, 48, 3528–3532.
(9) Frank, O.; Zehentbauer, G.; Hofmann, T.
Bioresponse-guided decomposition of roast coffee beverage and identification
of key bitter taste compounds.
Eur. Food Res. Technol. 2006, 222, 492–508.
(10) Frank, O.; Blumberg, S.; Kunert, C.; Zehentbauer, G.; Hofmann, T.
Structure determination and sensory analysis of bitter-tasting 4-vinylcatechol oligomers
and their identification in roasted coffee by means of LC-MS/MS.
J. Agric. Food Chem. 2007, 55, 1945–1954.
(11) Frank, O.; Blumberg, S.; Krümpel, G.; Hofmann, T.
Structure determination of 3-O-caffeoyl-epi-γ-quinide, an orphan bitter lactone in roasted coffee.
J. Agric. Food Chem. 2008, 56, 9581–9585.
(12) Trugo, L. C.; Macrae, R.
A study of the effect of roasting on the chlorogenic acid composition of coffee using HPLC.
Food Chem. 1984, 15, 219–227.
(13) Bennat, C.; Engelhardt, U. H.; Kiehne, A.; Wirries, F.-M.; Maier, H. G.
HPLC analysis of chlorogenic acid lactones in roasted coffee.
Z. Lebensm.-Unters. -Forsch. 1994, 199, 17–21.
(14) Schrader, K.; Kiehne, A.; Engelhardt, U. H.; Maier, H. G.
Determination of chlorogenic acids with lactones in roasted coffee.
J. Sci. Food Agric. 1996, 71, 392–398.
(15) Farah, A.; de Paulis, T.; Trugo, L. C.; Martin, P. R.
Effect of roasting on the formation of chlorogenic acid lactones in coffee.
J. Agric. Food Chem. 2005, 53, 1505–1513.
(16) Farah, A.; de Paulis, T.; Moreira, D. P.; Trugo, L. C.; Martin, P. R.
Chlorogenic acids and lactones in regular and water-decaffeinated Arabica coffees.
J. Agric. Food Chem. 2006, 54, 374–381.
(17) De Paulis, T.; Lovinger, D. M.; Martin, P.
Substituted Dicinnamoylquinides and their Use in Augmentation of Adenosine Function.
U.S. Patent 6693128 B2, 2004.
(18) Toelstede, S.; Hofmann, T.
Sensomics mapping and identification of the key bitter metabolites in Gouda cheese.
J. Agric. Food Chem. 2008, 56, 2795–2804.
(19) Stark, T.; Bareuther, S.; Hofmann, T.
Sensory-guided decomposition of roasted cocoa nibs (Theobroma cacao) and
structure determination of taste-active polyphenols.
J. Agric. Food Chem. 2005, 53, 5407–5418.
(20) Scharbert, S.; Holzmann, N.; Hofmann, T.
Identification of the astringent taste compounds in black tea infusions
by combining instrumental analysis and human bioresponse.
J. Agric. Food Chem. 2004, 52, 3498–3508.
(21) Glabasnia, A.; Hofmann, T.
Sensory-directed identification of taste active ellagitannins
in American (Quercus alba L.) and European oak wood (Quercus robur L.) and
quantitative analysis in bourbon whiskey and oak-matured red wines.
J. Agric. Food Chem. 2006, 54, 3380–3390.
'Coffee Chemistry' 카테고리의 다른 글
| 아라비카 커피의 쓴맛 화합물 Mozambioside (5) | 2025.05.10 |
|---|---|
| 새로 발견된 커피의 쓴맛 화합물 부류 (furan-2-yl)methylated benzene diols and triols (10) | 2025.05.08 |
| 커피의 쓴맛 (Bitter Taste of Roasted Coffee) (2) | 2025.05.06 |
| 커피의 쓴맛 물질 3-O-Caffeoyl-epi-γ-quinide (2) | 2025.05.05 |
| 커피 플레이버 화학의 수정 (4) | 2025.05.04 |




댓글